A B C D为短周期内除稀有气体外的元素 它们的原子序数依次增大.四种元素中只有C为金属元素;A和
| A、B、C、D为短周期内除稀有气体外的元素,它们的原子序数依次增大.四种元素中只有C为金属元素;A和C的最外层电子数相等;B、D属于同主族;C、D两元素原子的质子数之和为A、B两元素原子的质子数之和的3倍.请回答下列问题: (1)A的元素符号为______,B的原子结构示意图______. (2)C2B2中含有的化学键是______,写出C2B2与A2B反应的离子方程式______. (3)A、B、C、D离子半径由大到小的顺序为(用离子符号表示)______. (4)用化学方程式证明元素原子的得电子能力B强于D______. |
参考解答
| A、B、C、D为短周期内除稀有气体外的元素,它们的原子序数依次增大,C为金属元素;A和C的最外层电子数相等,位于同主族,则C为Na,A为H;B、D属于同主族,设B的质子数为x,则D的质子数为x+8,C、D两元素原子的质子数之和为A、B两元素原子的质子数之和的3倍,所以11+x+8=(1+x)×3,解得x=8,即B为O,D为S, (1)A为H,B为O,其原子结构示意图为 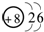 ,故答案为:H; 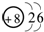 ; (2)C2B2为Na2O2,钠离子与过氧根离子以离子键结合,O、O之间以共价键结合,与水反应的离子反应为2Na2O2+2H2O═4Na++4OH-+O2↑, 故答案为:离子键、共价键;2Na2O2+2H2O═4Na++4OH-+O2↑; (3)电子层越多,离子半径越大,具有相同电子排布的离子,原子序数大的离子半径小, 则离子半径为S2->O2->Na+>H+, 故答案为:S2->O2->Na+>H+; (4)利用元素单质的置换反应可说明得电子能力的强弱,如H2S+O2═H2O+S↓,故答案为:H2S+O2═H2O+S↓. |
相似问题
下列说法正确的是( )A.在元素周期表中 元素所在族的族序数等于原子核外最外层电子数B.在元素周期
下列说法正确的是( )A.在元素周期表中,元素所在族的族序数等于原子核外最外层电子数B.在元素周期表中,元素所在的周期数等于原子核外电子数C.最
有X Y Z W四种短周期元素 原子序数依次增大.X的阳离子就是一个质子.Z W在周期表中处于相邻位
有X、Y、Z、W四种短周期元素,原子序数依次增大.X的阳离子就是一个质子.Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体.Y原子的最
已知由短周期元素组成的A B C D四种化合物所含原子数目依次为2 3 4 5 其中A B C含有1
已知由短周期元素组成的A、B、C、D四种化合物所含原子数目依次为2、3、4、5,其中A、B、C含有18个电子,D含有10个电子.请回答(1)A、B、D的化学式分别
K L M三种主族元素 已知K+和L-具有相同电子层结构 M元素原子核电荷数比L元素原子核电荷数少9
K、L、M三种主族元素,已知K+和L-具有相同电子层结构,M元素原子核电荷数比L元素原子核电荷数少9,L-在一定条件下可被氧化成LM3-,则下列说法正确的是(
观察下列A B C D E五种粒子(原子或离子)的结构示意图 回答有关问题:(1)属于离子结构示意图
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:(1)属于离子结构示意图的是______、______(填编号).(2)性质最稳定的原












