有X Y Z W四种短周期元素 原子序数依次增大.X的阳离子就是一个质子.Z W在周期表中处于相邻位
有X、Y、Z、W四种短周期元素,原子序数依次增大.X的阳离子就是一个质子.Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体.Y原子的最外层电子数是次外层电子数的2倍.请回答: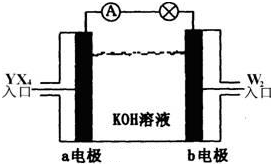 (1)Z2的电子式为______,Y的原子结构示意图为______,YW2的结构式为______. (2)将YX4、W2按上图所示通入某燃料电池中,则两极的电极方程式分别为: a电极:______,b电极:______.若有16gW2参加反应,转移的电子数是______. (3)已知在120℃、101kPa下,0.5mol X2在W2中完全燃烧时,释放出120.9kJ的热量,该反应的热化学方程式为______. (4)Y和Z结合可生成一种超硬物质,本身耐磨损,抗腐蚀,则该物质属于______晶体,该晶体中各粒子均满足8电子稳定结构,则化学式为______. |
参考解答
| X的阳离子就是一个质子,则X为H元素,Z、W在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体,只有Z为N元素,W为O元素符合,Y原子的最外层电子数是次外层电子数的2倍,则Y为C元素, (1)Z为N元素,单质为N2,为非金属单质,N原子之间有3个共用电子对,电子式为 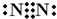 ,Y为C元素,原子核外有2个电子层,最外层电子数为4,原子结构示意图为 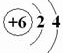 ,CO2为直线形分子,结构式为O=C=O, 故答案为: 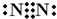 ;  ;O=C=O; (2)甲烷燃料电池中,甲烷为负极,发生反应为CH4-8e-+10OH-=CO32-+7H2O, 氧气为正极,电极反应为O2+4e-+2H2O=4OH-,16gO2的物质的量为
故答案为:CH4-8e-+10OH-=CO32-+7H2O;O2+4e-+2H2O=4OH-;2NA或1.204×1024; (3)已知在120℃、101kPa下,0.5mol X2在W2中完全燃烧时,释放出120.9kJ的热量,则1mol反应放出的热量为241.8KJ,热化学方程式为: H2(g)+1/2 O2(g)═H2O(g)△H=-241.8kJ?mol-1, 故答案为:H2(g)+1/2 O2(g)═H2O(g)△H=-241.8kJ?mol-1; (4)Y和Z结合可生成一种超硬物质,本身耐磨损,抗腐蚀,该晶体为原子晶体,化学式为C3N4,该晶体中各粒子均满足8电子稳定结构, 故答案为:原子;C3N4. |
相似问题
已知由短周期元素组成的A B C D四种化合物所含原子数目依次为2 3 4 5 其中A B C含有1
已知由短周期元素组成的A、B、C、D四种化合物所含原子数目依次为2、3、4、5,其中A、B、C含有18个电子,D含有10个电子.请回答(1)A、B、D的化学式分别
K L M三种主族元素 已知K+和L-具有相同电子层结构 M元素原子核电荷数比L元素原子核电荷数少9
K、L、M三种主族元素,已知K+和L-具有相同电子层结构,M元素原子核电荷数比L元素原子核电荷数少9,L-在一定条件下可被氧化成LM3-,则下列说法正确的是(
观察下列A B C D E五种粒子(原子或离子)的结构示意图 回答有关问题:(1)属于离子结构示意图
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:(1)属于离子结构示意图的是______、______(填编号).(2)性质最稳定的原
已知X+ Y2+ Z- W2-四种离子均具有相同的电子层结构.下列关于X Y Z W四种元素的描述
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构.下列关于X、Y、Z、W四种元素的描述,正确的是( )A.原子序数:Y>X>Z>WB.原子半径:X>Y
A B C D为原子序数小于18的四种元素:①A的原子的电子层数等于最外层电子数;②A与B处于同一周
A、B、C、D为原子序数小于18的四种元素:①A的原子的电子层数等于最外层电子数;②A与B处于同一周期,B与D可形成离子化合物D2B,该化合物的水溶液显碱性












