A B C E F为原子序数依次增大的六种元素 其中A B C D E为短周期元素 F为第四周期元素
| A、B、C、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素,F还是前四周期中电负极最小的元素。 已知: A原子的核外电子数与电子层数相等; B元素原子的核外p电子数比s电子数少1个; C原子的第一至第四电离能为I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol; D原子核外所有p轨道为全充满或半充满; E元素的族序数与周期序数的差为4; (1)写出E元素在周期表位置:________;D元素的原子的核外电子排布式:____________________。 (2)某同学根据题目信息和掌握的知识分析C的核外电子排布为 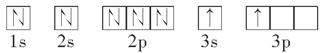 该同学所画的轨道式违背了________。 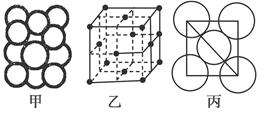 (3)已知BA5为离子化合物,写出其电子式:______________。 (4)DE3中心原子杂化方式为__________________,其空间构型为______________。 (5)某金属晶体中原子堆积方式如图甲,晶胞特征如图乙,原子相对位置关系如图丙,则晶胞中该原子配位数为________;空间利用率为________;该晶体的密度为________。(已知该金属相对原子质量为m,原子半径为a cm) |
参考解答
| (1)第三周期ⅦA族 1s22s22p63s23p3 (2)能量最低原理 (3) 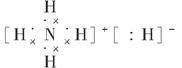 (4)sp3 三角锥形 (5)12 74% 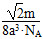 g/cm3 g/cm3 |
(1)由题意分析知F为K;A为H;B为N;由电离能知C的+2价稳定,为Mg;D为P;E为Cl。(2)原子的核外电子分能级排布,按构造原理先排能量低的能级,再排能量高的能级,遵循能量最低原理时,该原子才最稳定。该同学未排满3s能级,就排3p能级,违背了能量最低原理。(3)NH5为离子化合物,则为铵盐,存在NH4+和H-。(4)PCl3中心原子P上的价层电子对=3+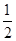 (5-3×1)=4,杂化类型为sp3杂化;存在一个孤电子对,故分子构型为三角锥形。(5)由图可知:该金属堆积方式为面心立方最密堆积,原子配位数为12,空间利用率为74%;由图乙可知每个晶胞中含有的原子数为8× (5-3×1)=4,杂化类型为sp3杂化;存在一个孤电子对,故分子构型为三角锥形。(5)由图可知:该金属堆积方式为面心立方最密堆积,原子配位数为12,空间利用率为74%;由图乙可知每个晶胞中含有的原子数为8×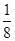 +6× +6×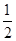 =4。设晶胞的棱长为x,由图丙知x2+x2=(4a)2,x=2 =4。设晶胞的棱长为x,由图丙知x2+x2=(4a)2,x=2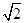 a,若该晶体的密度为ρ,则 a,若该晶体的密度为ρ,则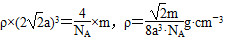 。 。点拨:本题考查物质结构与性质,考查考生对物质结构与性质的掌握情况。难度较大。 |
相似问题
卤族元素的单质和化合物很多 我们可以利用所学物质结构与性质的相关知识去认识和理解(1)卤族元素位于周
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解(1)卤族元素位于周期表的_________区;溴的价电子排布式为_______
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。(1)基态Ni原子的价电子(外围电子)排布式为
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。(1)基态Ni原子的价电子(外围电子)排布式为;(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子
在雷达的微波过滤器里使用铁氧磁性体为钇铁石榴石 (Y3Fe5O12) 其中Y最高正价为+3。下列有关
在雷达的微波过滤器里使用铁氧磁性体为钇铁石榴石 (Y3Fe5O12),其中Y最高正价为+3。下列有关叙述中正确的是[ ]A.可表示为3YO3·3FeO·Fe2O3 B.可表
【化学—选修3:物质结构与性质】(15分)氮化钛( Ti3N4)为金黄色晶体 由于具有令人满意的仿金
【化学—选修3:物质结构与性质】(15分)氮化钛( Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金代替品。以TiCl4为原料,经过
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是1
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示)。已知该分子中N—N—N键角都是108 1°,下列有关N(NO2)3的说法正确的是A.分子中N、O间形成












