纸包皮蛋是一项新技术 制作过程中需要配制料液。某配方料液中含NaOH NaCl 红茶末 五香粉等 技
| 纸包皮蛋是一项新技术,制作过程中需要配制料液。某配方料液中含NaOH、NaCl、红茶末、五香粉等,技术员先配得NaOH、NaCl的昆合液2400g,其中含80gNaOH,81gNaCl。计算: (1)混合液中NaOH的质量分数。 (2)如果取24g混合液,加入一定质量3.65%的稀盐酸恰好完全反应,计算所加稀盐酸的质量。 (3)24g混合液与稀盐酸反应后所得溶液中NaCl的质量分数。 |
参考解答
| 解:(l)混合溶液中氢氧化钠的质量分数为80g÷2400g=3.3% (2)设需要稀盐酸的质量为X,生存NaCl的质量为y NaOH + HCl == H2O + NaCl 40 36.5 58.5 80g÷2400g×24g 3.65%×X y 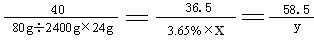 X=20g;y=1.17g (3)24g混合液与稀盐酸反应后所得溶液中NaCl的质量分数为 (1.17g+81g÷2400g×24g)÷(24g+20g)×100%==4.5% 答:(l)混合溶液中氢氧化钠的质量分数为3.3% (2)设需要稀盐酸的质量为20g (3)24g混合液与稀盐酸反应后所得溶液中NaCl的质量分数为4.5% |
相似问题
把16g氧气和12g碳放在密闭的容器里 在一定条件下充分反应 最终密闭容器中有[ ]A. B
把16g氧气和12g碳放在密闭的容器里,在一定条件下充分反应,最终密闭容器中有[ ]A B C D
为测定一瓶敞口放置的浓盐酸的溶质质量分数 某同学量取20mL(密度为1.1g/mL)的该盐酸与大理石
为测定一瓶敞口放置的浓盐酸的溶质质量分数,某同学量取20mL(密度为1 1g mL)的该盐酸与大理石充分反应,共用去含碳酸钙85%的大理石7 1g。(1)浓盐酸需要
某化学兴趣小组在做Fe和CuSO4溶液反应实验时 发现生成Cu的同时有气泡产生。为了进一步研究做了如
某化学兴趣小组在做Fe和CuSO4溶液反应实验时,发现生成Cu的同时有气泡产生。为了进一步研究做了如下实验:①取8 5gFe粉放入一定量的CuSO4中,反应完成后
把一定质量的锌和镁分别投入足量的稀盐酸中 充分反应后 生成氢气的质量关系如下图所示(图中m表示氢气的
把一定质量的锌和镁分别投入足量的稀盐酸中,充分反应后,生成氢气的质量关系如下图所示(图中m表示氢气的质量,t表示反应时间),则投入的锌和镁的质量
某实验小组用石灰石(杂质不与酸反应 也不溶于水)和稀盐酸反应制取二氧化碳 在准备将反应后的废液倒进废
某实验小组用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2












