现有前四周期A B C D E X六种元素 已知B C D E A五种非金属元素原子半径依次减小 其
| 现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题: (1)写出C、D、E三种原子第一电离能由大到小的顺序为______. (2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为______,根据价层电子对互斥理论预测BA2D的分子构型为______. (3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-.与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示)______ (4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如右图所示),其中3种离子晶体的晶格能数据如下表:
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是______. 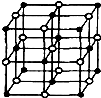 |
参考解答
| 根据B的s能级上电子总数等于p能级上电子总数的2倍,则电子排布式为:1s22s22p2,故为C,B、C、D、E、A五种非金属元素原子半径依次减小,,则为同周期,故B为N,C为O,D为F,A为H, (1)同周期从左到右第一电离能依次增大,但是在第ⅤA族的氮原子,p轨道上半充满状态稳定,不易失去电子,故答案为:F>N>O; (2)C、N、O原子的得电子能力O>N>C,得电子能力越强,其氢化物的稳定性越强,根据价层电子对互斥理论,NH2O的中心原子的杂化方式为sp2杂化,为平面三角形,故答案为:H2O>NH3>CH4;平面三角形; (3)X原子的M能层上有4个未成对电子,则电子排布式为:1s22s22p63s23p63d64s2,故为Fe,BC-为CN-,与A同族且相差两个周期的元素R即为Na,根据立方体结构,每个晶胞中含有钠、铁、和氢氰根的个数为:1、2、6,分子式为:NaFe2(CN)6,故答案为:NaFe2(CN)6; (4)晶格能越大则晶体熔点越高,则TiN>MgO>KCl,MgO晶体类型为立方体,其中一个Mg2+周围和它最邻近且等距离的O2-有6个,故答案为:TiN>MgO>KCl;6; (5)金属铬离子比钒离子Cr2O3含未成对电子多,则磁性大,磁记录性能越好,故答案为:Cr2O3. |
相似问题
已知A B C D E F都是周期表中前四周期的元素.它们的原子序数依次增大.其中A C原子的L层有
已知A、B、C、D、E、F都是周期表中前四周期的元素.它们的原子序数依次增大.其中A、C原子的L层有2个未成对电子.D与E同主族,D的二价阳离子与C的阴离子
甲 乙 丙 丁4种物质分别含2种或3种元素 它们的分子中各含18个电子 甲是气态氢化物 在水中分步电
甲、乙、丙、丁4种物质分别含2种或3种元素,它们的分子中各含18个电子,甲是气态氢化物,在水中分步电离出两种阴离子,下列推断合理的是( )A.某钠
A B C三种元素的原子具有相同的电子层数 而B的核电荷数比A大2 C原子的电子总数比B原子电子总数
A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子电子总数多4,1molA单质跟盐酸反应可置换出11 2L(标准状况下)
用A+ B- C2- D E F G分别表示含有18个电子七种微粒(离子或分子).回答:(1)A元素
用A+、B-、C2-、D、E、F、G分别表示含有18个电子七种微粒(离子或分子).回答:(1)A元素是______、B元素是______.B-的结构示意图为______、C元素是__
五种短周期元素有关数据如表.其中的X是表示元素原子在分子内吸引电子能力的大小 X越大 原子吸引电子的
五种短周期元素有关数据如表.其中的X是表示元素原子在分子内吸引电子能力的大小,X越大,原子吸引电子的能力越强,其最大值为4 0,最小值是0 7.试回答












