五种短周期元素有关数据如表.其中的X是表示元素原子在分子内吸引电子能力的大小 X越大 原子吸引电子的
五种短周期元素有关数据如表.其中的X是表示元素原子在分子内吸引电子能力的大小,X越大,原子吸引电子的能力越强,其最大值为4.0,最小值是0.7.试回答下列问题:
A.3.6B.3.1C.2.5D.1.4 (2)E元素在元素周期表中的位置是______,B元素单质的电子式为______. (3)A元素的原子最外层中有______个电子.A、B、C元素形成的单质中,结构微粒间作用力最强的是______(写物质名称). (4)用一个化学反应可以证明B和C非金属性的强弱,写出该反应的化学方程式:______. |
参考解答
| 五种短周期元素,A元素的主要化合价为-2价,没有正化合价,故A为O元素,B元素的主要化合价为+7价,故B为Cl元素,C元素的主要化合价为+6,故C为S元素,D元素化合价为+3,处于第ⅢA族,E元素化合价为+2,处于第ⅡA族,二者吸引电子能力相等,故二者不再同一周期,根据对角线原则,D为Al元素,E为Be元素, (1)同周期自左而右,元素原子吸引电子能力增强,故S元素的X值应介于Al与Cl之间,故选C; (2)E为Be元素,元素原子有2个电子层,最外层电子数为2,处于周期表中第二周期IIA族,B的单质为氯气,氯气分子中氯原子之间形成1对共用电子对,电子式为 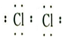 ,故答案为:第二周期IIA族; 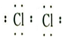 ; (3)A为O元素,最外层电子数为6,A、B、C元素形成的单质分别为氧气、硫单质、氯气,都属于分子晶体,常温下硫单质为固体,分子间作用力最强, 故答案为:6;硫; (4)利用氯气能置换硫单质即可证明氯元素的非金属性强于硫元素,方程式H2S+C12=2HC1+S可以证明,故答案为:H2S+C12=2HC1+S. |
相似问题
短周期元素A B C原子序数依次递增 它们的原子的最外层电子数之和为10.A与C在周期表中同主族 B
短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10.A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数.下列叙述正确
有A B C D四种元素 其中A元素和B元素的原子都有1个末成对电子 A+比B-少一个电子层 B原子
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个末成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个末成对电子,
A B C D四种短周期元素 A元素有三个电子层 其中最外层电子数占总电子数的1/6;B元素原子核外
A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的1 6;B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比
几种短周期元素的原子半径及主要化合价如下表:元素代号XYZW原子半径/pm1601437066主要化
几种短周期元素的原子半径及主要化合价如下表:元素代号XYZW原子半径 pm1601437066主要化合价+2+3+5、+3、-3-2下列叙述正确的是( )A.X、Y元素的金
几种短周期元素的原子半径及主要化合价见下表元素符号XYZRT原子半径(nm)0.1600.0800.
几种短周期元素的原子半径及主要化合价见下表元素符号XYZRT原子半径(nm)0 1600 0800 1020 1430 074主要化合价+2+2-2,+4,+6+3-2根据表中信息,判断以












