(10分)化学实验中 如使某步中的有害产物作为另一步的反应物 形成一个循环 就可不再向环境排放该种有
(10分)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如: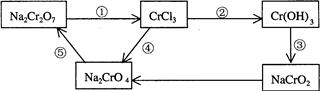 (l)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 (填编号)。 (2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是 (填化学式) (3)完成并配平步骤①的化学方程式,标出电子转移的方向和数目: □Na2Cr2O7+□KI+□HCl→□CrCl3+□NaCl+□KCl+□I2+□ |
参考解答
| (1)①、④(每空2分) (2)Cr(OH)3(2分) (3)1 6 14 2 2 6 3;7H2O(2分); 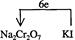 (2分) (2分) |
| (1)①中Cr的化合价由+6降低到+3,被还原,故要加入还原剂。④中Cr的化合价由+3升高到+6,故要加入氧化剂。 (2)由框图知,变化②和③中Cr的化合价没有改变,变化③是Cr(OH)3与NaOH的反应,而Cr(OH)3又可以看成是一种碱,故两性物质是Cr(OH)3 |
相似问题
实验室里迅速制备少量氯气可利用以下反应:______KMnO4+______ HCl═______
实验室里迅速制备少量氯气可利用以下反应:______KMnO4+______HCl═______KCl+______MnCl2+______Cl2↑+______H2O(1)请配平上述化学方程式,并在上面用
0.96 g Mg跟含6.3gHNO3的稀溶液恰好反应完全 则HNO3还原产物的式量是:A.30B.
0 96 g Mg跟含6 3gHNO3的稀溶液恰好反应完全,则HNO3还原产物的式量是:A.30B.44C.46D.80
(1)金属锰可以用四氧化三锰为原料通过铝热法来制备。试写出配平的化学方程式。(2)CS2是一种有恶臭
(1)金属锰可以用四氧化三锰为原料通过铝热法来制备。试写出配平的化学方程式。(2)CS2是一种有恶臭的液体,把它滴入硫酸酸化的高锰酸钾水溶液,将析出
配平并完成方程式。(1) Pt+ HNO3+ HCl H2PtCl6+ NO↑+
配平并完成方程式。(1) Pt+ HNO3+ HCl H2PtCl6+ NO↑+ ( )(2)Fe+ HNO3(稀) Fe(NO3)3+ NO↑+ H2O被还原与未被还原的氮元素质量之比。(3
钛(Ti)具有高强度和耐酸腐蚀性 是重要的工业原料.以金红石(主要成分为TiO2 含少量Fe2O3
钛(Ti)具有高强度和耐酸腐蚀性,是重要的工业原料.以金红石(主要成分为TiO2,含少量Fe2O3、SiO2)为原料可制取Ti.工业流程如下:(1)粗TiCl4中含有












