(6分)(1)已知拆开1molH-H键 lmolN-H键 1mol 键分别需要的能是436kJ 39
(6分)(1)已知拆开1molH-H键,lmolN-H键,1mol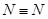 键分别需要的能是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。 键分别需要的能是436kJ、39lkJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________。(2)科学家盖斯曾提出:“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的。”利用盖斯定律可测某些特别反应的热效应。已知: 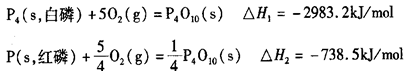 则白磷的稳定性比红磷_____________(填“高”或“低”),理由是________________ __________________________________________________________________________。 |
参考解答
 |
(1)化学反应的焓变等于反应物的总键能与生成物的总键能只差,所以反应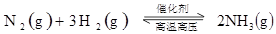 的焓变为 的焓变为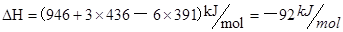 ,所以反应的热化学方程式为 ,所以反应的热化学方程式为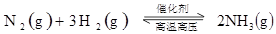 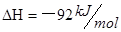 。 。(2)给热化学方程式 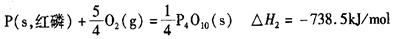 两边同时乘以4可以得到 两边同时乘以4可以得到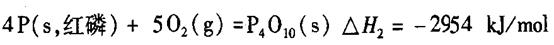 该式与白磷的热化学方程式相减可以得到 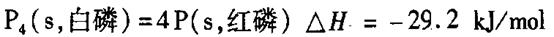 白磷生成红磷是放热反应所以红磷的能量低于白磷,能量越低越稳定,所以稳定性白磷低于于红磷。 |
相似问题
关于反应 下列说法正确的是A.反应前后 熵不变B.反应前后 分子总数不变C.反应前后 生成物总能量与
关于反应,下列说法正确的是A.反应前后,熵不变B.反应前后,分子总数不变C.反应前后,生成物总能量与反应物的总能量不变D.反应前后,氧元素化合价不变
(5分)有下列物质:①O2②CO2③HC1O ④Na2O ⑤Na2O2⑥NaOH ⑦H2O2⑧NH4
(5分)有下列物质:①O2②CO2③HC1O ④Na2O ⑤Na2O2⑥NaOH ⑦H2O2⑧NH4Cl,回答下列问题:⑴只含极性键的是---------------------------,⑵只含非极
(6分)某实验活动小组在实验室进行中和反应反应热的测定。请回答下列问题:(1)测定中和反应反应热的实
(6分)某实验活动小组在实验室进行中和反应反应热的测定。请回答下列问题:(1)测定中和反应反应热的实验装置如图所示。在两个烧杯之间填弃碎泡沫塑料
下图表示298K时N2与H2反应过程中的能量变化。根据下图叙述正确的是( )A.该反应的热化学方程
下图表示298K时N2与H2反应过程中的能量变化。根据下图叙述正确的是()A.该反应的热化学方程式为:1 2 N2(g)+3 2 H2(g)NH3(g) △H= -92kJ·mol-1B.
下列化合物既含有离子键又含有非极性共价键的是:A.Na2O2B.NaOHC.HClD.H2O2
下列化合物既含有离子键又含有非极性共价键的是:A.Na2O2B.NaOHC.HClD.H2O2












