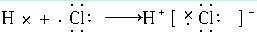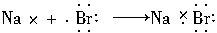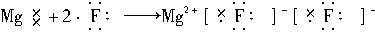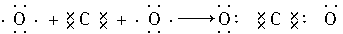参考解答
| D |
试题分析:A项中HCl的正确电子式为 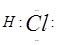 ,故A错误。 ,故A错误。NaBr为离子化合物,其电子式为 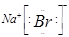 ,故B错误。 ,故B错误。C中MgF2电子为 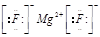 故C不正确。 故C不正确。D正确。 点评:考查物质形成过程的电子式书写格式,难度不大,注意对比离子化合物和共价化合物的电子式书写格式,即可解答。 |
相似问题
(8分)用价层电子对互斥理论判断下列物质的空间构型:① NH4+
(8分)用价层电子对互斥理论判断下列物质的空间构型:① NH4+ ② NH3 ③ CCl4④ SO3
下列关于化学键的叙述 正确的是( )A.构成单质分子的微粒之间一定存在共价键B.由非金属元素
下列关于化学键的叙述,正确的是( )A.构成单质分子的微粒之间一定存在共价键B.由非金属元素组成的化合物不一定是共价化合物C.共价键只存在于非金属元
根据下表中所列键能数据 判断下列分子中 最不稳定的分子是 化学键H—HH—ClH—ICl—ClB
根据下表中所列键能数据,判断下列分子中,最不稳定的分子是化学键H—HH—ClH—ICl—ClBr—Br键能 kJ mol436431299247193A. HCl B.HBr C.H2 D. Br2
已知:①H2(g)+O2(g)=H2O(g) △H1=a kJ·mol-1②2H2(g)+O2(g)
已知:①H2(g)+O2(g)=H2O(g)△H1=a kJ·mol-1②2H2(g)+O2(g)=2H2O(g)△H2=b kJ·mol-1③H2(g)+O2(g)=H2O(l)△H3=c kJ·mol-1④2H2(g)+O2
(7分)分别取40mL的0.50 mol/L盐酸与40mL的0.55 mol/L氢氧化钠溶液进行中和
(7分)分别取40mL的0 50 mol L盐酸与40mL的0 55 mol L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。(1)