在极性分子中 正电荷重心同负电荷重心间的距离称偶极长 通常用d表示。极性分子的极性强弱同偶极长和正(
| 在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极矩(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题: (1)HCl、CS2、H2S、SO2四种分子中μ=0的是___________________; (2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,3种分子的偶极矩由大到小的排列顺序是:___________________; (3)实验测得:μPF3=1.03、μBCl3=0。由此可知,PF3分子是___________构型,BC13分子是______________构型。 (4)治癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体,棕黄色者μ>0,淡黄色者μ=0。试画出两种异构体的构型图,并比较在水中的溶解度。构型图: |
 |
| 在水中溶解度较大的是___________________。 |
参考解答
| (1)CS2 (2)邻>间>对 (3)三角锥形;平面三角形 (4)  ; ;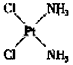 ;棕黄色者 ;棕黄色者 |
相似问题
下列说法中 正确的是( )A.离子化合物中一定不含共价键 共价化合物中一定不含离子键B.水分子呈直
下列说法中,正确的是( )A.离子化合物中一定不含共价键,共价化合物中一定不含离子键B.水分子呈直线形,氨分子呈三角锥形C.碳原子之间可形成碳碳
有两种配合物A和B 它们的组成为21. 95% Co 39.64% Cl 26.08%N 6.38%
有两种配合物A和B,它们的组成为21 95% Co,39 64% Cl,26 08%N,6 38%H,5 95%O,请根据下面的实验结果确定它们的配离子、中心离子、配位体和配位数
(1)请根据[Zn(NH3)4]2+中配位键的形成 总结配位键形成的条件。_____________
(1)请根据[Zn(NH3)4]2+中配位键的形成,总结配位键形成的条件。____________________ (2)在Fe3+、Cu2+、Zn2+、Ag+、H2O、NH3、F-、CN-、CO中,哪些可以
下列物质中 既有离子键 又有共价键和配位键的是( )A.HClB.Na2O2C.NH4ClD.KC
下列物质中,既有离子键,又有共价键和配位键的是( )A.HClB.Na2O2C.NH4ClD.KCl
金属及其化合物在生产 生活中有广泛应用.请回答下列问题:(1)工业上常利用Fe2+能与CN-形成稳定
金属及其化合物在生产、生活中有广泛应用.请回答下列问题:(1)工业上常利用Fe2+能与CN-形成稳定Fe(CN)4-6(六氰合亚铁离子)的特点来处理含CN-的工












