A B C D E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同 A与C
| A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同,A与E形成的化合物化学式为AE,其分子中含18个电子,请回答下列问题: (1)D元素的原子结构示意图为______. (2)由A、B、C三种元素形成的化合物的电子式为______,这种化合物形成的晶体中所含的化学键类型有______. (3)B、C、E三种元素形成一种盐,此盐中三种原子个数比为1:1:1,在25℃时,将该盐溶于水,测得溶液pH>7,理由是______(用离子方程式表示). |
参考解答
| A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,则A为氢元素;A与E形成的化合物化学式为AE,其分子中含18个电子,则E原子含有17个电子,故E为氯元素;A与C同主族,B和C的最外层电子数之和与E的最外层电子数相同,则B的最外层电子数为7-1=6,B与D分别为同主族,原子序数B小于D,则B为氧元素,D为硫元素;原子序数C等于氧元素,C与氢元素为同主族,故C为钠元素. (1)D为硫元素,原子核外电子数为16,有3个电子层,最外层电子数为6,原子结构示意图为 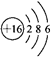 . 故答案为:  . (2)由A、B、C三种元素形成的化合物为NaOH,氢氧化钠是离子化合物,由钠离子与氢氧根离子构成,电子式为 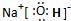 .晶体中钠离子与氢氧根离子之间形成离子键,氢氧根离子中氢原子与氧原子之间形成共价键. 故答案为: 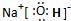 ;离子键、共价键. (3)B、C、E三种元素形成一种盐,此盐中三种原子个数比为1:1:1,该盐为NaClO,次氯酸钠属于强碱弱酸盐,在溶液中ClO-水解ClO-+H2O  HClO+OH-,使溶液呈碱性,溶液pH>7. 故答案为:ClO-+H2O  HClO+OH-. |
相似问题
元素X Y Z W均为短周期元素 且原子序数依次增大.已知Y原子最外层电子数占核外电子总数的 3/4
元素X、Y、Z、W均为短周期元素,且原子序数依次增大.已知Y原子最外层电子数占核外电子总数的3 4,W-、Z+、X+的离子半径逐渐减小,化合物XW常温下为气体
元素X和元素Y在周期表中位于相邻的两个周期 x与Y两原子核外电子总数之和为19 Y的原子核内质子数比
元素X和元素Y在周期表中位于相邻的两个周期,x与Y两原子核外电子总数之和为19,Y的原子核内质子数比X多3个.下列描述中不正确的是( )A.X与Y形成的
已知铬的核电荷数为24 以下是一些同学绘制的基态铬原子核外电子的轨道表示式(即电子排布图) 其 中最
已知铬的核电荷数为24,以下是一些同学绘制的基态铬原子核外电子的轨道表示式(即电子排布图),其 中最能准确表示基态铬原子核外电子运动状态的是 [ ]A B C D
X Y元素均为主族元素 aXm+和bYn-的电子层结构相同 下列叙述中错误的是( )A.Y的原子序
X、Y元素均为主族元素,aXm+和bYn-的电子层结构相同,下列叙述中错误的是( )A.Y的原子序数小于X的原子序数B.Y元素的核电荷数b等于a-m-nC.bYn-的
元素X的最高正价和最低负价的绝对值之差为6 Y元素的离子与X元素的离子具有相同的电子层结构 则X Y
元素X的最高正价和最低负价的绝对值之差为6,Y元素的离子与X元素的离子具有相同的电子层结构,则X、Y形成的化合物可能是( )A.MgF2B.K2SC.NaClD.KCl












