Ⅰ.某溶液中仅含下表离予中的5种离子(不考虑水的电离及离子的水解) 且各离子的物质的量均相等都为0.
Ⅰ.某溶液中仅含下表离予中的5种离子(不考虑水的电离及离子的水解),且各离子的物质的量均相等都为0.0lmol。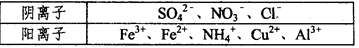 ①若向原溶液中加入KSCN溶液,无明显变化。 ②若向原溶液中加入过量的盐酸,有气体生成.溶液中阴离子种类不变。 ③若向原溶液中加入BaCl2溶液,有白色沉淀生成。 试回答下列问题 (1)若先向原溶液中先加入过量的盐酸,再加入KSCN溶液,现象是__________________。该过程中涉及的离子方程式有________________、__________________。 (2)向原溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体为____________________(写化学式)。 (3)向原溶液中加入足量盐酸后,用排水法收集所产生的气体并使气体恰好充满容器,将容器倒置于水槽中,再向容器中通入___________mLO2(气体体积均指标准状况),能使溶液充满该容器。 Ⅱ.amolCu2S和bmol FeS投入到v L c mol/L的稀硝酸中;充分反应,生成NO气体,所得澄清溶液可以看作Cu(NO3)2、Fe(NO3)3和H2SO4的混合溶液,则反应中未被还原的硝酸的物质的量为 ___________mol(用同时含有a、b、v、c的表达式表示)。 Ⅲ.已知CH4(g)+2O2(g)  CO2(g)+2H2O(l) △H1=a kJ/mol欲计算反应CH4(g)+4NO(g) CO2(g)+2H2O(l) △H1=a kJ/mol欲计算反应CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(l)的焓变△H2,则还需要查找某反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时△H3=b kJ/mol,则该反应的热化学方程式为______________________________________。 2N2(g)+CO2(g)+2H2O(l)的焓变△H2,则还需要查找某反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时△H3=b kJ/mol,则该反应的热化学方程式为______________________________________。据此计算出△H2=_____________kJ/mol(用含a和b的式子表示)。 |
参考解答
| I.(1)有气泡产生,溶液变成(血)红色(2分)(只要给出溶液变成(血)红色即得分) 3Fe2++4H++NO3-=3Fe3++NO↑+2H2O、Fe3++3SCN-= Fe(SCN)3(写成可逆符号给分)(2分) (2)Fe2O3、CuO(2分)(漏写一种得一分,有错写不给分)(其他合理答案也可) (3)56(2分) Ⅱ. 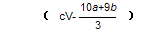 (2分) (2分)Ⅲ. N2(g) + O2(g)=2NO(g) △H3 =' b' kJ/mol (2分) a - 2b(2分) 或2NO(g)=N2(g) + O2(g) △H3 =' b' kJ/mol a +2b |
试题分析:依题意可以推出溶液中含有的离子种类应有Fe2+,NO3-,Cu2+ ,SO42-,Cl-。可以回答问题(1)。(2)应考虑Fe(OH)2在加热时生成Fe(OH)3,Cu(OH)2和Fe(OH)3在灼烧时生成Fe2O3、CuO。(3)因为4NO + 3O2 + 2H2O = 4HNO3,利用Fe2+的量为0.01mol,可以算出O2的体积。Ⅱ利用电子得失守恒可以推出被氧化的硝酸为 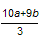 ,用硝酸的总量减去被氧化的硝酸可以求出。Ⅲ可以利用盖斯定律,欲计算反应CH4(g)+4NO(g) ,用硝酸的总量减去被氧化的硝酸可以求出。Ⅲ可以利用盖斯定律,欲计算反应CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(l),我们还需要知道N2与NO的关系。带入N2(g) + O2(g)=2NO(g) △H3 =' b' kJ/mol,△H2=△H1-2△H3 2N2(g)+CO2(g)+2H2O(l),我们还需要知道N2与NO的关系。带入N2(g) + O2(g)=2NO(g) △H3 =' b' kJ/mol,△H2=△H1-2△H3 |
相似问题
(6分)写出298K时 下列反应的热化学方程式(1)28 g CO还原Fe2O3生成单质铁 放出8.
(6分)写出298K时,下列反应的热化学方程式(1)28 g CO还原Fe2O3生成单质铁,放出8 3 kJ热量;(2)N2和O2化合生成184 g NO2气体,吸收热量135 4 kJ;
硫酸钠-过氧化氢-氯化钠加合物(xNaSO4·yH2O2·zNaCl)又称固体双氧水 是一种新型精细
硫酸钠-过氧化氢-氯化钠加合物(xNaSO4·yH2O2·zNaCl)又称固体双氧水,是一种新型精细化工产品,具有漂白、杀菌、消毒等作用。为探究该加合物的组成,
24mL0.5mol/LNa2SO3溶液 恰好与20 mL 0.2mol/LK2Cr2O7溶液完全反
24mL0 5mol LNa2SO3溶液,恰好与20 mL 0 2mol LK2Cr2O7溶液完全反应,则铬元素在还原产物中的化合价为A.+6B.+3 C.+2D.0
工业上以CuFeS2为原料冶炼铜的主要反应为①2CuFeS2+4O2Cu2S+3SO2+ 2FeO(
工业上以CuFeS2为原料冶炼铜的主要反应为①2CuFeS2+4O2Cu2S+3SO2+ 2FeO(炉渣);②2Cu2S+3O22Cu2O+2SO2;③2Cu2O+Cu2SCu+SO2↑。下列说法错误的
a mol FeS与b mol FeO投入到VL c mol/L的硝酸溶液中充分反应 产生NO气体
a mol FeS与b mol FeO投入到VL、c mol L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的












