(15分)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸 实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量
| (15分)硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾. ⑴SO2和O2反应制取SO3的反应原理为:2SO2+O2  2SO3,在一密闭容器中一定时间内达到平衡. 2SO3,在一密闭容器中一定时间内达到平衡.①该反应的平衡常数表达式为: . ②该反应达到平衡状态的标志是 . A.v(SO2)=v(SO3) B.混合物的平均相对分子质量不变 C.混合气体质量不变 D.各组分的体积分数不变 ⑵某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触. 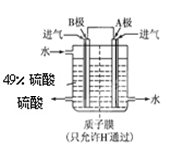 ①B电极的电极反应式为 ; ②溶液中H+的移动方向由 极到 极;(用A、B表示) ⑶测定绿矾产品中含量的实验步骤: a.称取5.7 g产品,溶解,配成250 mL溶液 b.量取25 mL待测液于锥形瓶中 c.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积40 mL 根据上述步骤回答下列问题: ①滴定时发生反应的离子方程式为(完成并配平离子反应方程式). Fe2++ 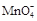 + —— Fe3++ Mn2++ + —— Fe3++ Mn2++ ②用硫酸酸化的KMnO4滴定终点的标志是 . ③计算上述产品中FeSO4·7H2O的质量分数为 . |
参考解答
⑴①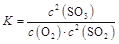 ②BD ②BD⑵①SO2+2H2O-2e-==SO42-+4H+ ②B A ⑶①5Fe2++1 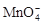 +8H+===5Fe3++1Mn2++4H2O +8H+===5Fe3++1Mn2++4H2O②滴定最后一滴酸性KMnO4时溶液呈淡紫色,半分钟内不褪色。 ③0.975或97.5% |
试题分析:(1)①根据平衡常数的概念可知 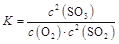 。 。②A项没有正逆反应速率,不能判断;B项混合物的平均相对分子质量反应前后不同,可以判断;C项混合气体的质量反应前后不变,不能判断;D项各组分的体积分数反应前后不同,可以判断。答案选BD。 (2)①根据B极的产物可以看出B极发生氧化反应,是负极,电极方程式为SO2+2H2O-2e-=SO42-+4H+。 ②阳离子向正极移动,所以H+从B极向A极移动。 (3)①根据化合价升降法,方程式配平为5Fe2++1 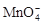 +8H+===5Fe3++1Mn2++4H2O。 +8H+===5Fe3++1Mn2++4H2O。②KMnO4本身有颜色,所以不需要指示剂,用本身的颜色就可以判断终点,当滴定最后一滴酸性KMnO4时溶液呈淡紫色,半分钟内不褪色时达到滴定终点。 ③产品中FeSO4·7H2O的质量分数为 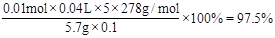 。 。点评:本题综合性强,难度较大,非常锻炼学生的思维能力。 |
相似问题
某氮的氧化物和CO在催化剂存在下充分反应 生成物质的量之比为1︰2的N2和CO2 该氧化物是(
某氮的氧化物和CO在催化剂存在下充分反应,生成物质的量之比为1︰2的N2和CO2,该氧化物是()A.N2OB.NOC.NO2D.N2O5
a g Fe粉与一定量的硝酸在一定条件下充分反应 将生成的气体与标准状况下b L 混合 恰好能被水
a g Fe粉与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b L 混合,恰好能被水完全吸收,则a和b的关系可能是A.b>0 3aB.b<0 2aC.0 2 3aD.无法确定
(4分)完成并配平下列化学方程式□FeO + □HNO3——□Fe(NO3)3 + NO↑+ □
(4分)完成并配平下列化学方程式□FeO + □HNO3——□Fe(NO3)3 + NO↑+ □,该反应中氧化剂是,当生成2mol NO时,转移的电子数为NA。
某金属单质与一定浓度的HNO3反应 假定只有单一的还原产物 当参加反应的单质与被还原的HNO3物质的
某金属单质与一定浓度的HNO3反应,假定只有单一的还原产物,当参加反应的单质与被还原的HNO3物质的量之比为3:2时,还原产物A.NO2 B.NO C.N2O D.N2
下列说法不正确的是A.金属单质与盐溶液的反应都是置换反应B.4Fe(OH)2+O2+2H2O=4Fe
下列说法不正确的是A.金属单质与盐溶液的反应都是置换反应B.4Fe(OH)2+O2+2H2O=4Fe(OH)3属于化合反应C.SO2+Cl2+2H2O=2HCl+H2SO4属于氧化还原反应D












