甲 乙 丙 丁 戊为原子序数依次增大的短周期元素.甲 丙处于同一主族 丙 丁 戊处于同一周期 戊的负
| 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、丙处于同一主族,丙、丁、戊处于同一周期,戊的负一价阴离子与丙的阳离子差8个电子。甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝;戊的单质与X反应能生成乙的单质,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1;丁的单质既能与丙元素最高价氧化物的水化物的溶液反应生成盐L也能与Z的水溶液反应生成盐N;丙、戊可组成化合物M。请回答下列问题: (1)戊离子的结构示意图为 。 (2)写出由甲乙两元素形成的化合物中,既含有极性键又含有非极性键的物质的结构式 ,该物质与空气在碱性条件下可构成燃料电池,该电池放电时,负极的反为 。 (3)戊的单质与X反应生成的Y和Z的物质的量之比为2:4,反应中被氧化的物质与被还原的物质的物质的量之比为 。 (4)写出少量Z的稀溶液滴入过量L的稀溶液中发生反应的离子方程式 。 (5)按如图电解M的饱和溶液: 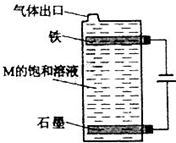 写出该电解池中发生反应的总反应方程式 。将充分电解后所得溶液逐滴加入到酚酞试液中,观察到得现象是 。 |
参考解答
(1)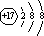 (2) 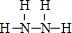 N2H4+4OH--4e-=N2↑+2H2O N2H4+4OH--4e-=N2↑+2H2O(3)2:3 (4)AlO2-+H++H2O═Al(OH)3↓ (5)2NaCl+H2O  NaClO+H2↑ 溶液变红后褪色 NaClO+H2↑ 溶液变红后褪色 |
| 甲、乙、丙、丁、戊为原子序数依次增大的短周期元素.甲、乙组成的常见气体X能使湿润的红色石蕊试纸变蓝,则X为NH3,甲为H,乙为N;甲、丙处于同一主族,结合原子序数可知,丙为Na;戊的负一价阴离子与丙的阳离子差8个电子,戊的负一价阴离子核外电子数为18,则戊为Cl;氯气与氨气反应生成氮气,同时生成两种溶于水均呈酸性的化合物Y和Z,0.1mol/L的Y溶液pH>1,则Y为NH4Cl、Z为HCl;丁的单质既能与丙(Na)元素最高价氧化物的水化物的溶液反应生成盐L,也能与Z(HCl)的水溶液反应生成盐N,丁为两性金属,则丁为Al元素,故L为NaAlO2;丙、戊组成化合物M为NaCl,用石墨作阳极、铁作阴极,电解氯化钠水溶液,生成氢气、氯气与氢氧化钠,氯气与氢氧化钠反应生成氯化钠与次氯酸钠。 (1)Cl-的结构示意图为: 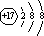 。 。(2)H、N两元素形成的化合物中,既含有极性键又含有非极性键的物质为N2H4,其结构式为 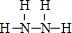 ,负极反应氧化反应,N2H4在负极失去电子,碱性条件下生成氮气与水,负极电极反应式为N2H4+4OH--4e-=N2↑+2H2O。 ,负极反应氧化反应,N2H4在负极失去电子,碱性条件下生成氮气与水,负极电极反应式为N2H4+4OH--4e-=N2↑+2H2O。(3)氯气与氨气反应生成的NH4Cl和HCl的物质的量之比为2:4,则NH3与Cl2反应的化学方程式:4NH3+3Cl2═N2+2NH4Cl+4HCl,在反应中氨气做还原剂,氯气做氧化剂,被氧化的物质氨气只占反应掉的一半,被氧化的物质氨气与被还原的物质氯气物质的量之比=2:3。 (4)将少量的盐酸滴入过量NaAlO2溶液中发生反应的离子方程式为:AlO2-+H++H2O═Al(OH)3↓。 (5)电解饱和氯化钠溶液,反应的方程式为:2NaCl+2H2O  2NaOH+Cl2↑+H2↑ , 2NaOH+Cl2↑+H2↑ ,同时发生反应Cl2+2NaOH=NaCl+NaClO+H2O,故该电解池中发生反应的总反应方程式为NaCl+H2O  NaClO+H2↑,电解后得到NaClO溶液,显碱性,且具有强氧化性,滴入酚酞溶液中,观察到溶液变红后褪色。 NaClO+H2↑,电解后得到NaClO溶液,显碱性,且具有强氧化性,滴入酚酞溶液中,观察到溶液变红后褪色。 |
相似问题
(6分)(2012?广东)如图是部分短周期元素化合价与原子序数的关系图 下列说法正确的是( )A.
(6分)(2012?广东)如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )A.原子半径:Z>Y>XB.气态氢化物的稳定性:R>WC.WX3
X Y Z是短周期的三种主族元素 在周期表中的相对位置如图所示 下列说法正确的是X YZ A.原子半
X、Y、Z是短周期的三种主族元素,在周期表中的相对位置如图所示,下列说法正确的是XYZA.原子半径:X<Y<ZB.X、Y、Z三种元素的最高价氧化物对应水化物
(15分)现有A B C D E F G H八种短周期主族元素 原子序数依次增大。已知A与E D与G
(15分)现有A、B、C、D、E、F、G、H八种短周期主族元素,原子序数依次增大。已知A与E、D与G分别同主族;E、F、G、H同周期;A分别与C、D可形成含有10个电
关于下列各组物质的相互关系 判断正确的是( )A.互为同素异形体的是①②B.互为同位素的是②③C
关于下列各组物质的相互关系,判断正确的是()A.互为同素异形体的是①②B.互为同位素的是②③C.互为同一物质的是①⑤D.互为同分异构体的是④⑤
下列叙述中错误的是 ( )A.原子半径:Cl>S>OB.还原性:Na>Mg>AlC.稳定性:HF
下列叙述中错误的是 ()A.原子半径:Cl>S>OB.还原性:Na>Mg>AlC.稳定性:HF>HCl>HBrD.酸性:HClO4>H2SO4>H3PO4












