(15分)月球含有H He N Na Mg Si等元素 是人类未来的资源宝库。(1)3He是高效核能
| (15分)月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。 (1)3He是高效核能原料,其原子核内中子数为_____________。 (2)Na的原子结构示意图为______,Na在氧气中完全燃烧所得产物的电子式为_______。 (3)MgCl2在工业上应用广泛,可由MgO制备。 ①MgO的熔点比BaO的熔点________(填“高”或“低”) ②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为______;SiO2的晶体类型为________。 ③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为______(写化学式)。 (4)月壤中含有丰富的3He,从月壤中提炼1 kg3He同时可得6000kgH2和700kgN2,若以所得H2和N2为原料经一系列反应最多可制得碳酸氢铵___kg。 |
参考解答
(1)1 (2)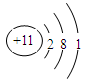 ; ;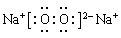 (3)①高 ②2OH-+SiO2=SiO32-+H2O;原子晶体 ③NaCl、NaClO、Na2CO3 (4)3950 |
试题分析:(1)在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数。因为质子数和中子数之和是质量数,因此该核素的原子核内中子数=3-2=1。 (2)原子结构示意图是表示原子核电荷数和电子层排布的图示形式。小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数。由于钠的原子序数是11,位于元素周期表的第三周期第IA族,因此钠的原子结构示意图为 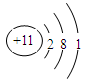 ;钠在氧气中完全燃烧生成过氧化钠,过氧化钠是含有离子键和非极性键的离子化合物,电子式可表示为 ;钠在氧气中完全燃烧生成过氧化钠,过氧化钠是含有离子键和非极性键的离子化合物,电子式可表示为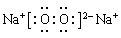 。 。(3)①氧化镁和氧化钡形成的晶体均是离子晶体,离子晶体的熔点与晶格能有关系。晶格能越大,熔点越高。形成离子键的离子半径越小,离子的电荷数越多离子键越强,晶格能越大。由于镁离子半径小于钡离子半径,因此氧化镁中晶格能大于氧化钡中晶格能,则氧化镁的熔点高于氧化钡的熔点。 ②氧化镁是碱性氧化物,二氧化硅是酸性氧化物,能与氢氧化钠溶液反应,而氧化镁与氢氧化钠溶液不反应,因此除去氧化镁中的二氧化硅可以用氢氧化钠溶液,反应的离子方程式为2OH-+SiO2=SiO32-+H2O;二氧化硅是由硅原子和氧原子通过共价键形成的空间网状结构的晶体属于原子晶体。 ③氧化镁、炭粉和氯气在一定条件下反应制备氯化镁,另一种生成物可以被氢氧化钠溶液完全吸收,则气体应该是二氧化碳,二氧化碳与足量的氢氧化钠溶液反应生成碳酸钠。另外过量的氯气有毒也需要尾气处理,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠,则盐的化学式为NaCl、NaClO、Na2CO3。 (4)根据反应的方程式可知 3H2 + N2 = 2NH3 6kg 28kg 34kg 6000kg 28000kg 34000kg 因此氮气不足,则实际生成的氨气的物质的量为 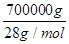 ×2,根据氮原子守恒可知,最终生成碳酸氢铵的质量为 ×2,根据氮原子守恒可知,最终生成碳酸氢铵的质量为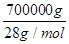 ×2×79g/mol=3950000g=3950kg。 ×2×79g/mol=3950000g=3950kg。 |
相似问题
(15分)X Y Z W R T为前四周期元素且原子序数依次增大。T原子序数等于X Y R原子序数之
(15分)X、Y、Z、W、R、T为前四周期元素且原子序数依次增大。T原子序数等于X、Y、R原子序数之和。Z为地壳中含量最多的元素。X、Z原子核外均有2个未成对
[物质结构与性质]含有NaOH的Cu(OH)2悬浊液可用于检验醛基 也可用于和葡萄糖反应制备纳米Cu
[物质结构与性质]含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O。(1)Cu+基态核外电子排布式为(2)与OH-互为等电子体的
J Q M R T是原子序数依次增大的短周期主族元素 J Q R在周期表中的相对位置如下表。已知J元
J、Q、M、R、T是原子序数依次增大的短周期主族元素,J、Q、R在周期表中的相对位置如下表。已知J元素最低负化合价的绝对值与其原子最外层电子数相等;M是
元素R有如下反应:RO+5R-+6H+===3R2+3H2O 下列说法正确的是( )A.元素R位
元素R有如下反应:RO+5R-+6H+===3R2+3H2O,下列说法正确的是()A.元素R位于周期表中第ⅤA族B.RO中的R只能被还原 C.每反应消耗1 mol RO,转移
已知aAn+ bB(n+1)+ cCn- dD(n+1)-具有相同的电子层结构 关于A B C D四
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是A.这四种离子的电子层结构相同,因而离子的性质也就












