有A B C D四种元素 A和B两种元素的原子各有两个电子层;C D两元素的原子各有三个电子层。A和
| 有A、B、C、D四种元素,A和B两种元素的原子各有两个电子层;C、D两元素的原子各有三个电子层。A和B能化合生成无色无味的气体AB2,C和D能化合生成C2D,B和D是同族元素,B离子和C离子核外电子数相同。 (1)这四种元素分别是:A ,B ,C ,D 。 (2)用电子式表示C和D形成化合物的过程: 。 |
参考解答
| (1)C O Na S (2) 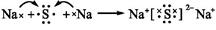 |
| 由AB2可推知B的化合价为-1或-2,由C2D可推知D化合价为-2或-4,B、D同族,则二者化合价为-2,即B、D为第ⅥA族元素,B为O,D为S;进而推知A为C,C为Na。 |
相似问题
C Si Ge Sn是同族元素 该族元素单质及其化合物在材料 医药等方面有重要应用.请回答下列问题:
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用.请回答下列问题:(1)32号元素Ge的原子核外电子排布式为 ;(2)C、S
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )元素代号ABDEG
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是()元素代号ABDEGIJK化合价–1–2+4–4–1+5–3+3+2+1原子半径/nm0.0710.074
下列说法正确的是( )。A.第二周期元素从C到F 非金属性逐渐减弱B.第三周期元素从Na到Cl 原
下列说法正确的是( )。A.第二周期元素从C到F,非金属性逐渐减弱B.第三周期元素从Na到Cl,原子半径逐渐增大C.HF、HCl、HBr、HI的热稳定性依次逐渐减弱
W X Y Z四种短周期元素在元素周期表中的相对位置如图所示 W的气态氢化物可使湿润的红色石蕊试纸变
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可使湿润的红色石蕊试纸变蓝,由此可知()A.X、Y、Z中最简单氢化物稳定性最
下列元素性质的递变规律正确的是( )A.原子半径:Be
下列元素性质的递变规律正确的是( )A.原子半径:Be<B<C<NB.第一电离能:B<Be<Mg<NaC.元素的电负性:O>N>P>SiD.气态氢化物的稳定性:NH3<CH4<PH3<SiH












