氯气 氨气等物质在生产和科研中都有重要应用.(1)若发生大量氯气泄漏事故 下列措施中正确的是____
| 氯气、氨气等物质在生产和科研中都有重要应用. (1)若发生大量氯气泄漏事故,下列措施中正确的是______. a.立即通报相关部门,迅速撤离事故现场 b.用蘸有肥皂水的毛巾捂住口鼻立即逆风疏散 c.用蘸有NaOH溶液的毛巾捂住口鼻立即顺风疏散 (2)事故发生后,可用NaOH稀溶液处理泄漏的氯气,反应的离子方程式是______. (3)实验室用氨气还原氧化铜的方法,通过测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)],测定铜的近似相对原子质量.反应的化学方程式是:2NH3+3CuO
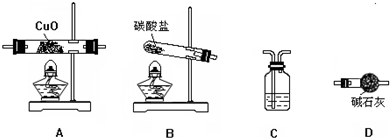 ①用上述装置制氨气时,能否将碳酸盐换成氯化铵?______(回答“是”或“否”),用化学方程式说明理由.______. ②仪器从左到右的连接顺序(用字母编号表示,仪器可重复使用)是______. C中的试剂是______,其作用是______. ③铜的相对原子质量是______[用含有m(CuO)、m(H2O)的式子表示]. (4)Cl2与NO2在一定条件下发生化合反应,生成一种气体,实验数据如图.图中横坐标是加入Cl2的物质的量,纵坐标是反应后气体物质的量总和.已知所取Cl2、NO2的物质的量总和为6mol.则生成物的化学式是______. 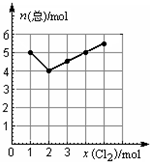 |
参考解答
| (1)氯气有毒,密度比空气大,易于碱性溶液反应,所以当氯气泄漏时立即通报相关部门,迅速撤离事故现场 ,NaOH具有较强的腐蚀性,应用用蘸有肥皂水的毛巾捂住口鼻而不能用NaOH溶液,并且逆风疏散,故答案为:a、b; (2)氯气与氢氧化钠溶液反应生成氯化钠和次氯酸钠,可用NaOH吸收尾气, 反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O; (3)①制备氨气时应用碳酸铵和氢氧化钙反应,而不能用氯化铵,因氯化铵分解生成的氨气和氯化氢气体易反应而重新生成氯化铵,反应的方程式为HCl+NH3=NH4Cl, 故答案为:否;HCl+NH3=NH4Cl; ②氨气还原氧化铜时,应先制备氨气,并用碱石灰干燥氨气,生成的氨气在加热条件下与氧化铜反应,生成的水用碱石灰吸收以测定生成水的质量,最后用浓硫酸吸收氨气并防止空气中的水和CO2进入D装置以免造成误差, 故答案为:BDADC;浓硫酸;防止空气中的水和CO2进入D装置,吸收多余的氨气; ③根据反应的方程式计算 2NH3+3CuO
3mol 3mol
M(CuO)=
故答案为:
(4)由图象可知:当氯气的物质的量为2mol时反应后气体的总物质的量最小,说明此时完全反应, 此时n(Cl):n(N02)=1:1,则有Cl2+2NO2═2NO2Cl,所以生成物为NO2Cl, 故答案为:NO2Cl. |
相似问题
下列化合物不能通过单质直接化合而制得的是( )A.CuCl2B.AlCl3C.FeCl2D.NaC
下列化合物不能通过单质直接化合而制得的是( )A.CuCl2B.AlCl3C.FeCl2D.NaCl
某研究性学习小组进行了一系列化学实验后 发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气
某研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,锰化合物的还原产物都是MnCl2(如:K2MnO4+8
下列说法正确的是( )A.光照氯水有气泡逸出 该气体是Cl2B.新制氯水呈黄绿色是因为其中存在Cl
下列说法正确的是( )A.光照氯水有气泡逸出,该气体是Cl2B.新制氯水呈黄绿色是因为其中存在Cl2C.久置氯水遇AgNO3溶液会产生白色沉淀D.新制氯水经
常温下能发生反应的一组气体是( )A.CH4 Cl2B.NH3 HClC.H2 Br2D.SO2
常温下能发生反应的一组气体是( )A.CH4、Cl2B.NH3、HClC.H2、Br2D.SO2、O2
已知Cl-和Ag+反应生成AgCl 每次新生成的AgCl中又有10%见光分解成单质银和氯气 氯气又可
已知Cl-和Ag+反应生成AgCl,每次新生成的AgCl中又有10%见光分解成单质银和氯气,氯气又可在水溶液中岐化成HClO3(为强酸)和HCl。而这样生成的Cl-又与剩












