A元素的最高价离子0.5 mol被还原成中性原子时 要得到6.02×1023个电子。它的单质同盐酸充
| A元素的最高价离子0.5 mol被还原成中性原子时,要得到6.02×1023个电子。它的单质同盐酸充分反应时,放出0.02 g H2,用去0.4 g A。B元素的原子核外电子层数与A相同,且B元素形成的单质是红棕色液体。 (1)写出这两种元素的名称:A ,B 。 (2)用结构示意图表示A、B两元素常见离子:A ,B 。 (3)用电子式表示A、B形成的化合物。 |
参考解答
| (1)钙 溴 (2)Ca2+ 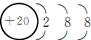 Br- Br-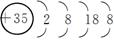 (3)  ∶-Ca2+ ∶-Ca2+ ∶- ∶- |
| 从B的单质为红棕色液体可推知B的单质为Br2。溴原子有4个电子层,所以A原子也有4个电子层,由0.5 mol A元素的最高价离子被还原成原子时能得到电子1 mol,说明A的离子为+2价,即A原子最外层有2个电子。 依题意:A ~ H2 M 2 0.4 g 0.02 g M=40 则A为钙元素。 |
相似问题
已知钾原子的原子结构示意图为:(如图所示)(1)钾元素的原子序数为:
已知钾原子的原子结构示意图为:(如图所示)(1)钾元素的原子序数为:(2)钾元素的原子在反应中易(填“得到”或“失去”)个电子,表现出性(填“氧
元素A的阳离子aAm+与元素B的阴离子bBn-具有相同的电子层结构。以下关于A B元素性质的比较中
元素A的阳离子aAm+与元素B的阴离子bBn-具有相同的电子层结构。以下关于A、B元素性质的比较中,正确的是①原子序数:A>B②离子半径:aAm+<bBn-③原
短周期元素A B C D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍 元素B在同周期的
短周期元素A、B、C、D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常
短周期元素甲 乙 丙 丁的原子序数依次增大 甲和乙形成的气态化合物的水溶液呈碱性 乙位于第VA族 甲
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等
下表是元素周期表的一部分 针对表中的①~⑩中元素 用元素符号或化学式回答以下问题: 主族周期I
下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式回答以下问题:主族周期IAIIAIIIAIVAVAVIAVIIA0二①②三③④⑤⑥⑦⑧四⑨⑩(1)












