对反应14CuSO4+5FeS2+12H­2O=7Cu2S+5FeSO4+12H2SO4的下
对反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4的下列说法正确的是
|
参考解答
| D |
试题分析:A、根据方程式可知硫酸铜中铜元素的化合价从+2价降低到+1价,得到1个电子,硫酸铜是氧化剂。FeS2中S元素的化合价从-1价部分升高到+6价,失去7个电子,做还原剂。部分从-1价降低到-2价,做氧化剂,A不正确;B、部分SO42-是氧化产物,B不正确;C、硫酸铜是氧化剂,因此1 mol CuSO4氧化了 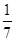 mol的S,C不正确;D、根据方程式和电子得失守恒可知,14mol硫酸铜氧化1mol FeS2。另外4mol FeS2中有3.5mol是氧化剂,0.5mol是还原剂,所以被还原的S和被氧化的S的质量比=3.5×2:(0.5×2+1×2)=7:3,D正确,答案选D。 mol的S,C不正确;D、根据方程式和电子得失守恒可知,14mol硫酸铜氧化1mol FeS2。另外4mol FeS2中有3.5mol是氧化剂,0.5mol是还原剂,所以被还原的S和被氧化的S的质量比=3.5×2:(0.5×2+1×2)=7:3,D正确,答案选D。 |
相似问题
(16分)MnO2与过量固体KOH和KClO3在高温下反应 生成锰酸钾(K2MnO4)和KCl K2
(16分)MnO2与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl,K2MnO4溶液经酸化后转化为MnO2和KMnO4。一种MnO2制备KMnO4的方法如下:(1
有Fe2+ Fe3+ H2O和H+六种粒子 分别属于同一氧化还原反应中的反应物和生成物 下列叙述
有Fe2+、、Fe3+、、H2O和H+六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是( )A.氧化剂与还原剂的物质的量之比为8∶1B.
汽车剧烈碰撞时 安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。则列判
汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。则列判断正确的是A.反应中KNO3为还原剂B.NaN3中氮元素为-3价C.标准状况下,若
工业上以铬铁矿(主要成分为FeO·Cr2O3) 碳酸钠 氧气和硫酸为原料生产重铬酸钠(Na2Cr2O
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应如下:①4FeO·Cr2O3+8Na2CO3+7O28Na2CrO4
将18 g铜和铁的混合物投入200 mL稀硝酸中 充分反应后得到标准状况下2.24 L NO 剩余9
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2 24 L NO,剩余9 6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又












