对金属表面进行处理 形成一层致密的氧化物保护膜 是非常有效的一种金属防腐技术.Ⅰ.钢铁“发蓝”是在钢
| 对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术. Ⅰ.钢铁“发蓝”是在钢铁表面形成一层致密的Fe3O4薄膜的技术.其中一种方法是将钢铁制品浸到NaNO2和浓NaOH的混合溶液中加热到130℃.其过程可以用如下化学方程式表示: ①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑ ②6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3↑+7NaOH ③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH 则反应②中的氧化剂是______(填化学式). Ⅱ.铝的阳极氧化,也是一种常用的金属表面处理技术,它能使铝的表面生成一层特别致密的氧化膜,该氧化膜不溶于稀硫酸.某化学研究小组在实验室中按下列步骤模拟该生产过程.请填写下列空白: (1)配制实验用的溶液.要配制500mL密度为1.2g?cm-3的溶质质量分数为16%的NaOH溶液,需要称取______g NaOH固体. (2)把铝片浸入热的16% NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗.写出除去氧化膜有关反应的离子方程式:______. (3)如图,组装好仪器,接通开关K,通电约25min.在阳极生成氧化铝,阴极产生气体.写出该过程中的电极反应式:阳极:______;阴极:______. 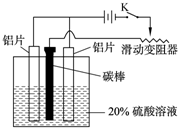 |
参考解答
| Ⅰ.反应②中,NaNO2中氮元素的化合价由+3价降为-3价,化合价降低的元素所在的反应物是氧化剂, 故答案为:NaNO2; Ⅱ、(1)NaOH的质量m=ρvw%=1.2g?cm-3×500mL×16%=96g,故答案为:96; (2)氧化铝是两性氧化物,能溶于强碱溶液,离子方程式为:Al2O3+2OH-═2AlO-2+H2O,故答案为:Al2O3+2OH-═2AlO-2+H2O; (3)电解池的阳极材料是铝时,则该电极反应是铝本身失电子的过程,即2Al+3H2O-6e-→Al2O3+6H+,阴极发生阳离子的得电子过程,在酸溶液中,为6H++6e-→3H2,故答案为:2Al+3H2O-6e-→Al2O3+6H+;6H++6e-→3H2↑. |
相似问题
下列物质中 按只有氧化性 只有还原性 既有氧化性又有还原性的顺序排列的一组是( )A.NO2 Na
下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是( )A.NO2、Na、Fe2+B.Cl2、Al、H2C.K+、F-、HClD.Na2O2、SO2、H2O
需加入还原剂才能发生的变化是( )A.Cl-→Cl2B.CO32-→CO2C.SO32-→SO42
需加入还原剂才能发生的变化是( )A.Cl-→Cl2B.CO32-→CO2C.SO32-→SO42-D.Fe3+→Fe2+
某一反应体系有反应物和生成物共五种物质:O2 H2CrO4 Cr(OH)3 H2O H2O2.已知该
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中,H2O2只发生如下过程:H2O2-→O2.(1)该反应的还原剂是___
下列反应中必须加入氧化剂才能进行的是( )A.KClO3→O2B.Cu2+→CuC.Fe2+→Fe
下列反应中必须加入氧化剂才能进行的是( )A.KClO3→O2B.Cu2+→CuC.Fe2+→Fe3+D.CuO→CuCl2
已知:还原性HSO-3>I- 氧化性IO-3>I2.在含3mol NaHSO3的溶液中逐滴加入KIO
已知:还原性HSO-3>I-,氧化性IO-3>I2.在含3molNaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如右图所示.下列有关说法正确












