Ⅰ.请把符合要求的化学方程式的字母填在下列空白处:①既属于分解反应 又属于氧化还原反应的是_____
| Ⅰ.请把符合要求的化学方程式的字母填在下列空白处: ①既属于分解反应,又属于氧化还原反应的是______. ②属于分解反应,但不属于氧化还原反应的是______. ③既属于化合反应,又属于氧化还原反应的是______. ④属于化合反应,但不属于氧化还原反应的是______. ⑤不属于四种基本反应类型的氧化还原反应的是______. A.(NH4)2SO3
B.2CO+O2
C.2C+SiO2
D.NH4NO3
E.CaCO3+CO2+H2O=Ca(HCO3)2 F.MnO2+4HCl(浓)
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为______. (2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气. ①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O ②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂______mol,被氧化的物质的质量为______ g. |
参考解答
Ⅰ、A、(NH4)2SO3
B.2CO+O2
C.2C+SiO2
D.NH4NO3
E.CaCO3+CO2+H2O=Ca(HCO3)2 ;反应是化合反应,不是氧化还原反应; F.MnO2+4HCl(浓)
故答案为:Ⅰ.①D ②A ③B ④E ⑤F Ⅱ.(1)依据氧化还原反应的电子守恒计算,根据化合价升降分析,8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,该反应中氧化剂与还原剂的物质的量之比为5:2,标注化合价求化合价升降判断氧化剂还原剂,还原剂:2Mn2+~2MnO4-~10e-;氧化剂:5R2O8n-~10RO42-~(20-5n)e-,依据电子守恒得到:10=20-5n,n=2,故答案为:2; (2)①用单线桥表示出该反应的电子转移情况为: 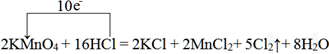 故答案为: 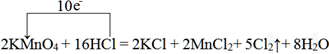 ; ②反应为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O;在标准状况下,该反应产生2.24L Cl2时物质的量为0.1mol,氧化剂为KMnO4,2KMnO4~5Cl2,消耗氧化剂KMnO4为0.04mol;被氧化的物质为HCl,氧化剂和还原剂的定量关系为:2KMnO4~10HCl,所以被氧化的氯化氢物质的量为0.2mol,氯化氢的质量=0.2mol×36.5g/mol=7.3g; 故答案为:0.04;7.3. |
相似问题
下列叙述中正确的是( )A.有X变为X2-的反应是氧化反应B.凡有单质参与的化学反应 一定是氧化还
下列叙述中正确的是( )A.有X变为X2-的反应是氧化反应B.凡有单质参与的化学反应,一定是氧化还原反应C.含氧酸能发生氧化反应,无氧酸则不能D.反
已知反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 请回答下列问题:(1)请用双线
已知反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,请回答下列问题:(1)请用双线桥法标出电子转移的方向和数目______(2)上述反应中,______元素被氧化,_
金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS2+O2=Cu
金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS2+O2=Cu2S+2FeS+SO2,下列说法不正确的是( )A.O2只做氧化剂B
水热法制备纳米颗粒Y(化合物)的反应为:3Fe2++2S2O32-+O2+aOH-═Y+S4O62-
水热法制备纳米颗粒Y(化合物)的反应为:3Fe2++2S2O32-+O2+aOH-═Y+S4O62-+2H2O下列说法中,不正确的是( )A.S2O32-是还原剂B.Y的化学式为Fe2O3C
往FeCl3和BaCl2的混合溶液中通入SO2 溶液颜色由棕黄色变成浅绿色 同时有白色沉淀产生.下列
往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生.下列说法正确的是( )A.该实验表明FeCl3有还原性B.白色沉












