我国化工专家侯德榜 勇于创新 改进氨碱法设计了“联合制碱法” 为世界制碱工业作出了突出贡献。请完成下
| 我国化工专家侯德榜,勇于创新,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。请完成下列问题: (1)“联合制碱法”制得的“碱”是 (填化学式)。 (2)氨碱法和联合制碱法是两大重要的工业制碱法,下列表达中,不正确的是 。
某实验小组,利用下列装置模拟“联合制碱法”。 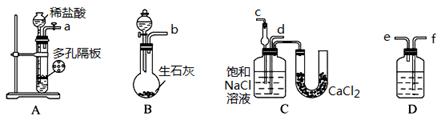 (3)取上述仪器连接装置,顺序为:(a)接( )、( )接( );(b)接( ); 检验气密性后装入药品,应该先让 装置(填上述字母)先发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体。 (4)C中用球形干燥管而不用直导管,其作用是 ,D中应选用的液体为 ; (5)C中广口瓶内产生固体的总化学方程式为 。 (6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为: (注明你的表达式中所用的有关符号的含义)。 |
参考解答
| (1)Na2CO3 (2)A.C (3)f e d c (2分) B (4)防倒吸 饱和NaHCO3溶液 (5)CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl (6) 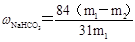 ( m1为样品质量,m2为加热后产品的质量) ( m1为样品质量,m2为加热后产品的质量) |
试题分析:(1)“联合制碱法”制得的“碱”是碳酸钠,化学式为Na2CO3。 (2)A、氨碱法原料有:食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气,联合制碱法原料有:食盐、氨气、二氧化碳,故A错误;B、氨碱法可能的副产物为氯化钙,联合制碱法可能的副产物氯化铵,故B正确;C、氨碱法循环物质:氨气、二氧化碳,联合制碱法循环物质:氯化钠,二氧化碳,故C错误;D、氨碱法原料(食盐和石灰石)便宜,产品纯碱的纯度高,副产品氨和二氧化碳都可以回收循环使用,制造步骤简单,适合于大规模生产,但设备复杂;能耗高,氨碱法的最大缺点还在于原料食盐的利用率只有72%~74%;联合制碱法最大的优点是使食盐的利用率提高到96%以上,废弃物少,故D正确,答案选AC。 (3)A装置是制备CO2,B装置是制备NH3,由于氨气极易溶于水需要用干燥管防止倒吸,另外CO2中的氯化氢气体还需要除去,因此正确的连接顺序为(a)接(f)、(e)接(d);(b)接(c)。由于CO2在水中的溶解度小,因此要首先产生氨气,然后再通入CO2气体,所以应该先让B装置先发生反应。 (4)氨气极易溶于水,因此C中用球形干燥管而不用直导管的作用是防倒吸。除去CO2中的氯化氢气体应该用饱和NaHCO3溶液,即D中应选用的液体为饱和NaHCO3溶液。 (5)C装置是制备碳酸氢钠的,所以C中广口瓶内产生固体的总化学方程式为CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl。 (6)设m1为样品质量,m2为加热后产品的质量,则根据碳酸氢钠分解的方程式可知 2NaHCO3 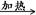 Na2CO3+H2O+CO2↑ 固体质量减少△m Na2CO3+H2O+CO2↑ 固体质量减少△m168g 106g 62g X m1-m2 解得X= 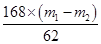 所以纯碱中碳酸氢钠的质量分数可表示为 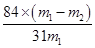 。 。 |
相似问题
钾(K)与Na在性质上具有很大的相似性 但K比Na的活泼性强 下面是根据Na的性质对K的性质的预测
钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的 [ ]A.因为K的活泼性强,所以钾应该保存在
(8分)取100mL FeCl3 AlCl3的混合溶液 逐滴加入物质的量浓度为1 mol·L-1的N
(8分)取100mL FeCl3、AlCl3的混合溶液,逐滴加入物质的量浓度为1 mol·L-1的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液的体积(单位为mL)关系如
下列有关钠的物理性质的叙述正确的是[ ]①银白色金属 ②质软 可以用小刀切割 ③熔点低于10
下列有关钠的物理性质的叙述正确的是[ ]①银白色金属 ②质软,可以用小刀切割 ③熔点低于100℃ ④密度比水小 ⑤热和电的良导体 A.①②④B.①②③
按图装置通入X气体 并在管P处点燃 实验结果是澄清石灰水变浑浊 则X Y可能是 ( )。A.H2
按图装置通入X气体,并在管P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可能是 ( )。A.H2和Fe2O3B.CO和CuOC.H2和Na2CO3D.CO和Na2CO3
切开的金属Na暴露在空气中 其变化过程如下:(1)反应Ⅰ的反应过程与能量变化的关系如下:① 反应Ⅰ
切开的金属Na暴露在空气中,其变化过程如下:(1)反应Ⅰ的反应过程与能量变化的关系如下:① 反应Ⅰ 是 反应(填“放热”或“吸热”),判断依据












