下图所示装置中 甲 乙 丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液 足量的CuSO4溶
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。 |
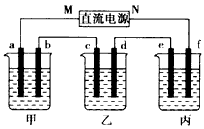 |
| (1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10. 47%,乙中c电极质量增加。据此回答问题: ①电源的N端为_________极; ②电极b上发生的电极反应为______________________; ③列式计算电极b上生成的气体在标准状况下的体积:_____________________ ④电极c的质量变化是______________________g; ⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因: 甲溶液________________________ 乙溶液________________________ 丙溶液________________________ (2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么? _______________________________ |
参考解答
(1)①正;②4OH--4e-==2H2O+O2;③水减少的质量: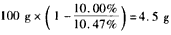 ,生成O2体积: ,生成O2体积: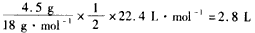 ;④16; ;④16;⑤甲溶液:碱性增大,因为电解后,水量减少,溶液中NaOH浓度增大 乙溶液:酸性增大,因为阳极上OH-生成O2,溶液中H+离子浓度增加 丙溶液:酸碱性大小没有变化,因为K2SO4是强酸强碱盐,浓度增加不影响溶液的酸碱性 (2)能继续进行,因为CuSO4溶液已转变为H2SO4溶液,反应也就变为水的电解反应 |
相似问题
在一定条件下利用电解的方法可以将含有少量的Fe Zn Cu Pt等金属杂质的粗镍提纯.下列叙述正确的
在一定条件下利用电解的方法可以将含有少量的Fe、Zn、Cu、Pt等金属杂质的粗镍提纯.下列叙述正确的是(已知氧化性:Fe2+<Ni2+<Cu2+)( )A.纯镍作
按图a中装置进行实验 图中两电极均为银棒 若图b的X轴表示流入电极的电子的量 则Y轴不可能表示的情况
按图a中装置进行实验,图中两电极均为银棒,若图b的X轴表示流入电极的电子的量,则Y轴不可能表示的情况是( )A.c(Ag+)B.c(NO3-)C.溶液的pHD.银棒质量
某同学按下图所示的装置进行实验。A B为两种常见金属 它们的硫酸盐可溶于水。当K闭合时 在交换膜处S
某同学按下图所示的装置进行实验。A、B为两种常见金属,它们的硫酸盐可溶于水。当K闭合时,在交换膜处SO42-从右向左移动。下列分析正确的是[ ]A.溶液中
某溶液中含有两种溶质NaCl和H2SO4 它们的物质的量之比为3:1.滴入几滴石蕊溶液后 用石墨作电
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1.滴入几滴石蕊溶液后,用石墨作电极电解该混合溶液,根据电极产物,电解过程可明显分为三个
按图的装置连接好仪器 先在烧杯中加入20mL左右的氢氧化钡溶液 再滴入几滴酚酞试液 接通电源后 逐渐
按图的装置连接好仪器,先在烧杯中加入20mL左右的氢氧化钡溶液,再滴入几滴酚酞试液,接通电源后,逐渐滴加稀硫酸.(1)当向烧杯中逐渐滴加稀硫酸时,烧












