下列叙述正确的是A.P4和NO2都是共价化合物B.CCl4和NH3都是以极性键结合的极性分子C.在C
下列叙述正确的是
 |
参考解答
| C |
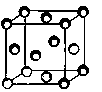
试题分析:A、P4是由P原子构成的单质,不是化合物,A不正确;B、四氯化碳属于正四面体型结构,是以极性键结合的非极性分子,B不正确;C、氧化钙是形成的晶体类型是离子晶体,由阴阳离子构成。二氧化硅形成的晶体类型是原子晶体,由原子构成,均不存在单个的小分子,C正确;D、根据铜晶胞的结构并依据均摊法可知,该晶胞中铜原子个数=8× 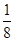 +6× +6×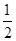 =4个,D不正确,答案选C。 =4个,D不正确,答案选C。 |
相似问题
试判断下列哪组原子中 所有原子核内的质子数或中子数为奇数[ ]A. B. C.元素周期表中I
试判断下列哪组原子中,所有原子核内的质子数或中子数为奇数[ ]A. B. C.元素周期表中IA族所有元素的原子 D.元素周期表中第3周期所有元素的原子
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子 其分子结构如右图
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示。已知断裂1 mol N—N吸收167 kJ热量,生成1 mol NN
下列叙述正确的是( )A.分子晶体中都存在共价键B.F2 C12 Br2 I2的熔沸点逐渐升高与
下列叙述正确的是()A.分子晶体中都存在共价键B.F2、C12、Br2、I2的熔沸点逐渐升高与分子间作用力有关C.含有极性键的化合物分子一定不含非极性键D.
1803年 英国科学家道尔顿提出了近代原子学说 他认为一切物质是由原子构成的 这些原子是微小的不可分
1803年,英国科学家道尔顿提出了近代原子学说,他认为一切物质是由原子构成的,这些原子是微小的不可分割的实心球。1911年,英国科学家卢瑟福用一束平行
下列对分子及性质的解释中 不正确的是( ) A.碘易溶于四氯化碳 甲烷难溶于水都可用相似相溶原
下列对分子及性质的解释中,不正确的是( ) A.碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释B.由于乳酸()中存在一个手性碳原子,导致该物












