(1)在配合物Fe(SCN)2+中 提供空轨道接受孤对电子的微粒是___________ 画出配合物
| (1)在配合物Fe(SCN)2+中,提供空轨道接受孤对电子的微粒是___________,画出配合物离子 [Cu(NH3)4]2+中的配位键________。 (2)根据VSEPR模型,H3O+的分子立体结构为:____________,BCl3的立体结构为:_____________。 (3)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式:(各写一种) 正四面体分子_________,三角锥形分子__________,V形分子____________。 |
参考解答
(1)Fe3+;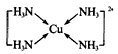 |
| (2)三角锥形;正三角形 (3)CH4(或CF4);NH3(或NF3);H2O(或H2S) |
相似问题
某分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构 原子间以单键相连。下列有关
某分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是[ ]A.X原子可能为VA族元素 B
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体。顺铂的结构式为 具有抗癌作用;
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体。顺铂的结构式为,具有抗癌作用;反铂的结构式为,无抗癌作用。(1)C、N、O三种元素的电负
下列物质中 分子的立体构型与水分子相似的是 [ ]A. CO2B. H2S C. PCl3D
下列物质中,分子的立体构型与水分子相似的是 [ ]A CO2B H2S C PCl3D SiCl4
已知A B C D E都是周期表中前四周期的元素 它们的核电荷数A<B<C<D<E。其中A B C是
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC形成的晶体为离子晶体,D的
配离子[Cu(NH3)4]2+中 中心离子的配位数是[ ]A.1B.2C.4D.6
配离子[Cu(NH3)4]2+中,中心离子的配位数是[ ]A.1B.2C.4D.6












