一定温度下 可逆反应A2(s)+3B2(g) 2AB3(g)在可变容器中不能作为达到平衡的标志是A
一定温度下,可逆反应A2(s)+3B2(g) 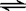 2AB3(g)在可变容器中不能作为达到平衡的标志是 2AB3(g)在可变容器中不能作为达到平衡的标志是
|
参考解答
| B |
| A 能作为标志,能体现出正、逆反应速率相等 B 不能作为标志,达到平衡时,各物质的物质的量之比不一定等于化学计量数之比 C 能作为标志,因为此反应是一个物质的量发生变化的反应。 D 能作为标志,密度=质量/体积,气体质量不变,但气体的体积是不断变化的,当体积不变时,反应达到平衡。故选B |
相似问题
哈伯因发明了用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2
哈伯因发明了用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在高温高压催化剂共存的条件下使该反应发生
在一固定容积的容器中进行如下反应:H2(g)+ I2(g) 2HI(g) 下列情况一定能说明反应已达
在一固定容积的容器中进行如下反应:H2(g)+ I2(g) 2HI(g),下列情况一定能说明反应已达到限度的是A.H2、 I2、HI的浓度之比为1 : 1 : 2时B.气体
(9分)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应2SO2(g)+O
(9分)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应2SO2(g)+O2(g)2SO3(g)过程中的能量变化如图所示,回答下列问题。(1)T℃时
(15分)某经济开发区将钛冶炼厂与氯碱厂 甲醇厂组成了一个产业链(如图所示) 大大地提高了资源利用率
(15分)某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大地提高了资源利用率,减少了环境污染。请填写下列空白:(1)写出钛
恒温(1100℃)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g)→Na2S(s)+4H2O
恒温(1100℃)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g)→Na2S(s)+4H2O(g)。下列说法正确的是( )A.该反应的平衡常数表达式K=c(H2O) c(H2)B.若容












