(14分)某学生设计氨催化氧化实验 并将制得的NO进一步氧化为NO2 用水吸收NO2 并检验HNO3
| (14分)某学生设计氨催化氧化实验,并将制得的NO进一步氧化为NO2,用水吸收NO2,并检验HNO3的生成。 可供选择的固体药品有:NH4Cl、Ca(OH)2、KClO3、MnO2、CaO 可供选择的液体药品有:浓氨水、过氧化氢、浓盐酸、水 可供选择的仪器有:如图 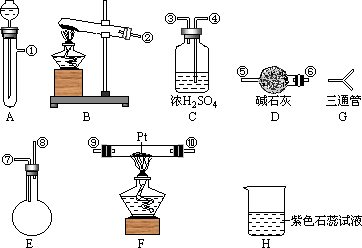 另有铁架台、铁夹、铁圈、乳胶管若干,可供选择。设计实验时,A和B两个制气装置允许使用两次,其余装置只能使用一次。 (1)氨氧化制NO的化学反应方程式为 ,该反应应在装置_______中进行。 (2)为快速制NH3和O2,制取NH3的装置最好选择_______________,其化学反应方程式为__________ ;制取O2的装置最好选择_______,其化学反应方程式为_____________。 (3)利用快速制NH3和O2的装置组装,各仪器按气流方向连接的正确顺序为____________(按装置先后顺序排列) (4)装置C的作用是___________________。 (5)装置H中溶液变红,其原因是(用化学方程式表示)______________________。 |
参考解答
25.(14分)(1)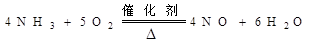 ;(2分) F (1分) ;(2分) F (1分)(2)A;(1分) NH3·H2O(浓)+CaO=NH3↑+Ca(OH)2 (2分) A;(1分) 2H2O2 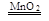 2H2O+O2↑ (2分) 2H2O+O2↑ (2分)(3) 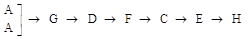 (2分) (2分)(4)吸收多余NH3及生成 H2O (1分) (5)4NO2+O2+2H2O=4HNO3 (2分) |
试题分析:(1)氨氧化制NO的化学反应方程式为 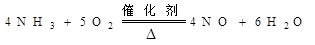 。由于是两种气体之间的反应,所以根据装置的特点可知,应该放在装置F找进行。 。由于是两种气体之间的反应,所以根据装置的特点可知,应该放在装置F找进行。(2)要快速制备氨气,则应该是将生石灰加入到浓氨水中,所以选择的装置是A,反应的化学方程式是NH3·H2O(浓)+CaO=NH3↑+Ca(OH)2。 (3)由于生成的氨气和氧气中都含有水蒸气,且反应后剩余的氨气要被浓硫酸吸收,同时还要干燥NO,所以正确的连接顺序是 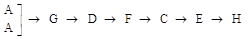 (4)根据以上分析可知,装置C中浓硫酸的作用是吸收多余NH3及生成 H2O。 (5)由于NO2和剩余的氧气溶于水会有硝酸生成,溶液显酸性,因此石蕊试液变为红色,反应的离子方程式是4NO2+O2+2H2O=4HNO3。 点评:该题是中等难度的试题,试题综合性强,贴近高考,侧重对学生实验能力的培养和训练。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。 |
相似问题
下列各组混合物 可以用分液漏斗分离的是A.甲苯和水B.甲苯和苯C.溴乙烷与水D.苯与溴乙烷
下列各组混合物,可以用分液漏斗分离的是A.甲苯和水B.甲苯和苯C.溴乙烷与水D.苯与溴乙烷
下列实验操作中错误的是( )A.分液时 分液漏斗中下层液体从下口放出 上层液体从上口倒出B.蒸馏
下列实验操作中错误的是()A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出B.蒸馏时,应该使温度计的水银球靠近蒸馏烧瓶支管口略下一点C
23(12分)实验室有一瓶碳酸钠试剂 含有少量的硫酸钠杂质 某学生设计以下实验来确定其纯度。A.称取
23(12分)实验室有一瓶碳酸钠试剂,含有少量的硫酸钠杂质,某学生设计以下实验来确定其纯度。A.称取样品W1 gB.加盐酸酸化C.用蒸馏水溶解D.过滤E 加
下列实验能成功的是:①用水鉴别NaHCO3和Na2CO3固体;②用观察法区别Na2O和Na2O2;③
下列实验能成功的是:①用水鉴别NaHCO3和Na2CO3固体;②用观察法区别Na2O和Na2O2;③用稀盐酸鉴别NaAlO2和AlCl3溶液;④用稀盐酸鉴别NaHCO3和Na2CO3溶液
某课外活动小组对一氧化碳还原氧化铁的实验中最后的产物产生浓厚的兴趣 试通过实验来探究其成分。Ⅰ.实验
某课外活动小组对一氧化碳还原氧化铁的实验中最后的产物产生浓厚的兴趣,试通过实验来探究其成分。Ⅰ.实验装置:用一氧化碳还原氧化铁的实验装置该装置B












