图所示是验证氯气性质的微型实验 a b d e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后
图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O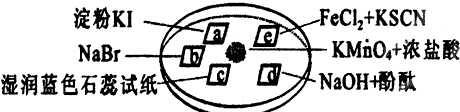 对实验现象的“解释或结论”正确的是( )
|
参考解答
| A、Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变橙色,可证明氧化性:Cl2>I2、Cl2>Br2,无法证明I2与Br2之间氧化性的强弱,故A错误; B、氯气与水反应Cl2+H2O=H++Cl-+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则C处先变红,后褪色,能证明氯气与水生成了酸性物质和漂白性物质,故B错误; C、Cl2和氢氧化钠反应生成氯化钠、次氯酸钠和水,消耗了氢氧化钠红色退去,不能证明生成物质具有漂白性,故C错误; D、Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2=2Fe3++2Cl-;Fe3++3SCN-=Fe(SCN)3,证明还原性Fe2+>Cl-,故D正确; 故选D. |
相似问题
将按等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中 再滴入含有品红和Ba(NO3)2的混
将按等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,再滴入含有品红和Ba(NO3)2的混合溶液,则发生的实验现象是( )A.红色溶液很快褪色B
将由CaCO3 MgCO3组成的混合物充分加热至质量不再减少时 称得残留物的质量为原混合物的一半 则
将由CaCO3、MgCO3组成的混合物充分加热至质量不再减少时,称得残留物的质量为原混合物的一半,则残留物中Ca、Mg两元素原子的物质的量之比是多少?
变色眼镜的玻璃镜片内含有少量溴化银和微量氧化铜.当玻璃受到阳光照射时 因为发生_________反应
变色眼镜的玻璃镜片内含有少量溴化银和微量氧化铜.当玻璃受到阳光照射时,因为发生_________反应(用化学方程式表示,下同),而使玻璃由无色变成灰黑色
下列说法错误的是( )A.钠和铁一样 都能在氯气中燃烧生成金属氯化物B.液氯是氯气的水溶液 它能使
下列说法错误的是( )A.钠和铁一样,都能在氯气中燃烧生成金属氯化物B.液氯是氯气的水溶液,它能使干燥的有色布条褪色C.氯气跟变价金属反应生成高
下列实验现象的描述错误的是( )A.CuSO4溶液不能产生丁达尔现象 Fe(OH)3胶体能产生丁达
下列实验现象的描述错误的是( )A.CuSO4溶液不能产生丁达尔现象,Fe(OH)3胶体能产生丁达尔现象B.向石蕊试液中加入新制氯水,石蕊试液变红后一直












