纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去) 向饱和CaCl2溶液中通入N
| 纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙. 供选择的药品: ①石灰石 ②氯化铵 ③氢氧化钙 ④饱和氯化钙溶液 ⑤浓硫酸 ⑥6mol?L-1盐酸⑦饱和食盐水⑧饱和NaHCO3溶液 (1)装置A中,仪器a的名称是______,仪器b中发生反应的离子方程式为______.装置D的试管中发生反应的化学方程式为______.装置B中盛放的溶液是______(填药品序号). (2)设计一个简单的实验方案,判断所得碳酸钙颗粒是否为纳米级.______.(简述实验的步骤、现象和结论) (3)通入适量气体后,C装置中物质恰好完全反应,过滤,所得滤液显______(填“酸”、“碱”、“中”之一)性,原因是______(用离子方程式表示). (4)上述装置存在一处缺陷,该缺陷为______. 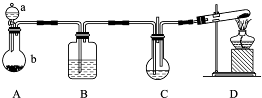 |
参考解答
(1)仪器a的名称是分液漏斗;仪器b中为碳酸钙与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑;装置D中制取氨气,化学方程式为2NH4Cl+Ca(OH)2
(2)将少量碳酸钙加水充分搅拌,看是否有丁达尔效应,若有丁达尔效应,则说明为纳米级,故答案为:将少量碳酸钙加水充分搅拌,用一束可见光照射,观察是否发生丁达尔现象,若有丁达尔现象则为纳米级,若没有丁达尔现象则不是纳米级; (3)氯化铵在水中发生水解显酸性,离子方程式:N
(4)该装置尾气未处理,故答案为:无尾气吸收装置. |
相似问题
下列离子方程式书写正确的是 [ ]A.钠和冷水反应 Na+2H2O=Na++2OH-+H
下列离子方程式书写正确的是 [ ]A.钠和冷水反应Na+2H2O=Na++2OH-+H2↑ B.铝粉投入到NaOH溶液中:2Al+2OH-══2AlO2-+H2↑ C.AlCl3溶液中加入足量
将Cu片放入0.1mol/L FeCl3溶液中 反应一定时间后取出Cu片 此时在溶液中有c (Fe3
将Cu片放入0 1mol LFeCl3溶液中,反应一定时间后取出Cu片,此时在溶液中有c(Fe3+):c(Fe2+)=2:3,则Fe3+与Cu2+的物质的量之比为多少?
在Al2(SO4)3和MgSO4的混合溶液中 滴加NaOH溶液 生成沉淀的量与滴入NaOH溶液的体积
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原来混合溶液中Al2(SO4)3和MgSO4的物质的量浓度
硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌 菱锌矿的主要成分是ZnCO3 并含少量的
硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3MgO、CaO等,生产工艺流程示意如下:(
下列各组反应 前后均可用同一离子方程式表示的是( )A.HCl+Na2CO3 HCl+NaHCO3
下列各组反应,前后均可用同一离子方程式表示的是( )A.HCl+Na2CO3,HCl+NaHCO3B.H2S+NaOH,H2SO4+KOHC.HCl+Na2CO3,H2SO4+K2CO3D.BaCl2+Na2SO4,BaCO3+H2SO4












