自然界存在NaIO3 可利用NaIO3与NaHSO3溶液来制取单质碘。反应分两步进行:IO3-+3
自然界存在NaIO3,可利用NaIO3与NaHSO3溶液来制取单质碘。反应分两步进行:IO3-+3HSO3-=I-+3SO42-+3H+;IO3-+5I-+6H+=3I2+3H2O。下列说法错误的是( )
|
参考解答
| D |
试题分析:A选项正确,IO3-中I的价态+5价到产物I-,价态降低,作氧化剂。HSO3-中S的价态由+4价到产物SO42-中+6价的S,价态升高,作还原剂。B选项正确,在第一步反应中产物有SO42-生成。因环境中阳离子有H+和 Na+,所以可以得到副产物H2SO4和Na2SO4。C选项正确。D选项错误。HSO3-作为还原剂其还原性应大于还原产物I- 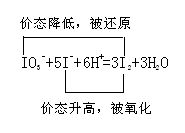 |
相似问题
(6分)向含有Cl- Br- I- Fe2+的溶液中 加入足量的溴水 反应后溶液中离子数量明显减少的
(6分)向含有Cl-、Br-、I-、Fe2+的溶液中,加入足量的溴水,反应后溶液中离子数量明显减少的是;离子数量基本不变的是。
含有a mol FeBr2的溶液中 通入 x mol Cl2。下列各项为通Cl2过程中 溶液内发生反
含有a mol FeBr2的溶液中,通入 x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是 ( )A.x=0 4a,2Fe2++Cl2=2Fe
在下列反应中 硫元素表现出还原性的是( )A.稀硫酸与锌粒反应B.三氧化硫与水反应C.浓硫酸与铜
在下列反应中,硫元素表现出还原性的是()A.稀硫酸与锌粒反应B.三氧化硫与水反应C.浓硫酸与铜反应D.二氧化硫与氧气反应
物质氧化性 还原性的强弱 不仅与物质的结构有关 还与物质的浓度和反应温度有关 下列各组物质:①Cu与
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关,下列各组物质:①Cu与浓硝酸;②Fe与浓硫酸;③Na与氧气;④PO与水,
在常温下 发生下列几种反应①2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
在常温下,发生下列几种反应①2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O ②Cl2+2NaBr=2NaCl+Br2 ③Br2+2FeBr2=2FeBr3根据上述反应,下列结论正确的是(












