建筑工地常用的NaNO2因外观和食盐相似 又有咸味 容易使人误食中毒。已知NaNO2能发生如下反应:
| 建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2 能发生如下反应: 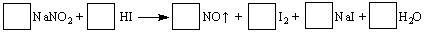 (1)配平上述反应方程式,将系数填入方框中。 (2)上述反应的氧化剂是 ,若反应中有5 mol电子转移,则生成NO在标准状况下的体积是 L。 (3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:①水;②碘化钾淀粉试纸;③淀粉;④白酒;⑤食醋,进行实验,下列几组合适的是 。
|
参考解答
| (1)2NaNO2 + 4HI =2NO + I2 +2 NaI +2 H2O (2)NaNO2;112 (3)C |
试题分析:(1)根据得失电子守恒法配平方程式,亚硝酸钠中N为+3价,反应后降为+2价;HI中I为-1价,反应后成为单质升高为0价,所以答案为2NaNO2 + 4HI =2NO + I2 +2 NaI +2 H2O; (2)氧化剂是元素化合价降低的物质,所以氧化剂是NaNO2;每生成1molNO,则转移1mol电子,若反应中有5 mol电子转移,则生成5molNO,标准状况下的体积是112L; (3)根据(2)可知,亚硝酸钠在酸性条件下,可以氧化碘离子为碘单质,碘遇淀粉变蓝色,所以选择的一组试剂是C。 |
相似问题
有Fe3+ Fe2+ NO3- NH4+ H+和H2O六种微粒 分别属于一个氧化还原反应中的反应物和
有Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述中,不正确的是A.还原产物为NH4+B.氧化剂与还原
(1)氧化还原反应的实质是___________________。(2)铁跟氯气在点燃条件下发生反应
(1)氧化还原反应的实质是___________________。(2)铁跟氯气在点燃条件下发生反应:2Fe+3Cl22FeCl3,其中氯元素的化合价_______(填“升高”或“降低
下列实验过程中 始终无明显现象的是( )A.NO2通入FeSO4溶液中B.CO2通入CaCl2溶液
下列实验过程中,始终无明显现象的是( )A.NO2通入FeSO4溶液中B.CO2通入CaCl2溶液中C.NH3通入AlCl3溶液中D.SO2通入已酸化的Ba(NO3)2溶液中
下列说法正确的是[ ]A. 摩尔是物质的量的单位 B. 氧化还原反应的本质是元素化合价发生了
下列说法正确的是[ ]A 摩尔是物质的量的单位 B 氧化还原反应的本质是元素化合价发生了变化C 熔融状态下或溶液中能导电的物质就是电解质 D 得
NaH是一种离子化合物 它跟水反应的方程式为:NaH+H2O═NaOH+H2↑ 它也能跟液氨 乙醇等
NaH是一种离子化合物,它跟水反应的方程式为:NaH+H2O═NaOH+H2↑,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气.下列有关NaH的叙述错误的是(












