Ⅰ.这两年全省范围均加大了严查酒后驾车的力度.对于司机酒后驾车 可对其呼出的气体进行检查而查出 所利
| Ⅰ.这两年全省范围均加大了严查酒后驾车的力度.对于司机酒后驾车,可对其呼出的气体进行检查而查出,所利用的化学反应如下: 2CrO3 (红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O,被检测的气体成分是______,上述反应中化合价降低的元素是______,化合价升高的元素是______. Ⅱ.“绿色试剂”双氧水可作为采矿业废液消毒剂,如果要消除采矿业废液中的氰化物(如KCN),化学反应方程式为:KCN+H2O2+H2O=A+NH3↑. (1)生成物A的化学式为______; (2)反应中发生氧化反应的物质为______; (3)H2O2被称为绿色氧化剂的理由是______. (4)用单线桥表示出该反应电子转移的方向和数目______; 当有2.5mol NH3生成时,共转移电子______个. Ⅲ.某溶液中含有H+、Mg2+、Fe2+、S2-、I-等微粒,已知还原性S2->I->Fe2+,只有氧化性的是______,只有还原性的是______,既有氧化性又有还原性的是______.往溶液中加入镁粉,最后得到的还原产物是______,往溶液中通入Cl2,最先得到的氧化产物是______(填化学式). |
参考解答
| Ⅰ.由题意知,被检测的物质是乙醇;该反应2CrO3 (红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O中,元素的化合价变化如下:CrO3→Cr2(SO4)3,Cr元素由+6价→+3价,得电子化合价降低;C2H5OH→CH3CHO,C元素由-2价→-1价,失电子化合价升高. 故答案为:C2H5OH;Cr;C; Ⅱ.(1)根据原子守恒得生成物A的化学式为KHCO3 ,故答案为:KHCO3 ; (2)KCN→KHCO3,C元素由+2价→+4价,KCN失电子作还原剂,发生氧化反应,故答案为;KCN; (3)双氧水发生反应后生成水,对环境无污染,故答案为:反应后一般被还原为水,无污染; (4)该反应中转移2个电子; KCN+H2O2+H2O=KHCO3+NH3↑ 转移电子 1mol 2NA 2.5mol 5 NA 故答案为: 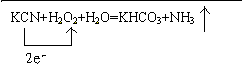 ; 5NA; Ⅲ.最高价态元素只有氧化性,最低价态只有还原性,中间价态既有氧化性又有还原性,所以只有氧化性的是H+、Mg2+;只有还原性的是S2-、I-;既有氧化性又有还原性的是Fe2+; 往溶液中加入镁粉,镁作还原剂,H+、Fe2+作氧化剂,但 H+的氧化能力大于Fe2+的氧化能力,所以后得到的还原产物是Fe;往溶液中通入Cl2,Cl2作氧化剂,Fe2+、S2-、I-有还原性,还原性S2->I->Fe2+,所以最先得到的氧化产物是S. 故答案为:H+、Mg2+;S2-、I-;Fe2+;Fe;S. |
相似问题
Ⅰ.高炉炼铁过程中发生的主要反应为:13Fe2O3(s)+CO(g)?23Fe(s)+CO2(g)已
Ⅰ.高炉炼铁过程中发生的主要反应为:13Fe2O3(s)+CO(g)?23Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:温度 ℃100011501300平衡常数4 0
ClO2是一种常用的预防“禽流感”的消毒剂 可通过以下反应制得(未配平):KClO3+H2C2O4+
ClO2是一种常用的预防“禽流感”的消毒剂,可通过以下反应制得(未配平):KClO3+H2C2O4+H2SO4→ClO2↑+K2SO4+CO2↑+H2O下列说法正确的是( )A.H2SO
某元素在化学反应中由游离态变为化合态 则该元素( )A.一定被氧化B.一定被还原C.既不可能被氧化
某元素在化学反应中由游离态变为化合态,则该元素( )A.一定被氧化B.一定被还原C.既不可能被氧化,又不可能被还原D.既可能被氧化,又可能被还原
从铝土矿制备铝所涉及的下列有关反应中 属于氧化还原反应的是( )A.铝土矿溶于NaOH溶液中B.偏
从铝土矿制备铝所涉及的下列有关反应中,属于氧化还原反应的是( )A.铝土矿溶于NaOH溶液中B.偏铝酸钠溶液的酸化C.灼烧氢氧化铝固体D.电解熔融的氧化铝
已知将浓盐酸滴入高锰酸钾溶液中 产生黄绿色气体 而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有
已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有3Cl、Cl2、H2SO4、H2O、3MnO4、MnSO4、32SO4七












