某一反应体系中 MnO2+4HCl=MnCl2+2H2O+Cl2↑.(1)该反应中的氧化剂是____
| 某一反应体系中,MnO2+4HCl=MnCl2+2H2O+Cl2↑. (1)该反应中的氧化剂是______. (2)标出电子转移的方向和数目:______. (3)该反应中,氧化剂与还原剂的物质的量之比为______. (4)若产生的气体在标准状况下体积为2.24L,则反应过程中转移电子的数目为______. |
参考解答
| (1)因反应中二氧化锰中的Mn元素的化合价降低,则二氧化锰为氧化剂,故答案为:MnO2; (2)该反应中Cl元素失去电子,Mn元素得到电子,转移的电子总数为2e-,则电子转移的方向和数目 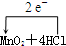 (浓)═MnCl2+Cl2↑+2H2O,故答案为: 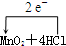 (浓)═MnCl2+Cl2↑+2H2O; (3)由MnO2+4HCl=MnCl2+2H2O+Cl2↑可知,1molMnO2反应时氧化剂为1mol,但参加反应的4molHCl中只有 2molHCl作还原剂,即氧化剂与还原剂的物质的量之比为1:2,故答案为:1:2; (4)标准状况下体积为2.24L氯气其物质的量为
由MnO2+4HCl=MnCl2+2H2O+Cl2↑~2e-可知,生成0.1molCl2时,转移的电子数为0.1×2×NA=0.2NA(或写为1.204×1023),故答案为:0.2NA(或写为1.204×1023). |
相似问题
下列反应既是离子反应 又是氧化还原反应的是( )A.氯化钠溶液中滴入硝酸银溶液B.氢气还原氧化铜C
下列反应既是离子反应,又是氧化还原反应的是( )A.氯化钠溶液中滴入硝酸银溶液B.氢气还原氧化铜C.铁片置于硫酸铜溶液中D.一氧化碳的燃烧
下列说法正确的是( )A.金属单质在反应中只能作还原剂 非金属单质只能作氧化剂B.Cl2溶于水形成
下列说法正确的是( )A.金属单质在反应中只能作还原剂,非金属单质只能作氧化剂B.Cl2溶于水形成的溶液能导电,所以Cl2是电解质C.二氧化硅不与水反
已知:6.4克铜与适量的浓硝酸反应 当铜完全溶解后 共收集到NO和NO2混合气体共2.24升(已折算
已知:6 4克铜与适量的浓硝酸反应,当铜完全溶解后,共收集到NO和NO2混合气体共2 24升(已折算为标准状况).求:(1)被还原的HNO3的物质的量;(2)参
工业上常用Fe2O3 和CO反应冶炼铁 该反应中( )A.氧化剂是COB.氧化剂是Fe2O3C.氧
工业上常用Fe2O3和CO反应冶炼铁,该反应中( )A.氧化剂是COB.氧化剂是Fe2O3C.氧化剂是FeD.还原剂是CO2
下列生活中的化学现象与氧化还原知识有关的是( )A.菜刀洗过后如果没擦干放置一段时间就会出现斑点B
下列生活中的化学现象与氧化还原知识有关的是( )A.菜刀洗过后如果没擦干放置一段时间就会出现斑点B.用食醋可以洗水垢C.蔗糖放在水中片刻后消失了












