我国化学家侯德榜改革国外的纯碱生产工艺 生产流程可简要表示如图(1)上述生产纯碱的方法称 副
我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如图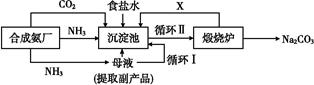 (1)上述生产纯碱的方法称 ,副产品的一种用途为 。 (2)沉淀池中发生的化学反应方程式是 。 (3)写出上述流程中X物质的分子式 。 (4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作是 。 (5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。 (6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。 a.增大NH4+的浓度,使NH4Cl更多地析出 b.使NaHCO3更多地析出 c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度 |
参考解答
| (1)联合制碱法或侯德榜制碱法 用作化肥或电解液或焊药等(其他合理答案均给分) (2)NH3+CO2+H2O+NaCl  NH4Cl+NaHCO3↓ NH4Cl+NaHCO3↓(3)CO2 (4)I 过滤 (5)稀硝酸和硝酸银溶液 (6)ac |
本题主要考查侯氏制碱法的生产原理及生产工艺、Cl-检验等。(1)侯氏制碱法的副产物是NH4Cl,可作化肥等;(2)根据联合制碱法的生产原理,可知向食盐水中通入氨气是为了得到碱性溶液,以吸收更多的CO2,当CO2过量时发生反应:NH3+CO2+H2O NH4HCO3,NaCl+NH4HCO3 NH4HCO3,NaCl+NH4HCO3 NaHCO3↓+NH4Cl;(3)当NaHCO3在煅烧炉中受热分解:2NaHCO3 NaHCO3↓+NH4Cl;(3)当NaHCO3在煅烧炉中受热分解:2NaHCO3 Na2CO3+CO2↑+H2O,故X为CO2;(4)因为氯化钠最后剩余在母液中,所以要提高NaCl的利用率必须将过滤出NaHCO3后的母液循环利用;(5)要检验碳酸钠中是否混有NaCl,只需向溶液中加硝酸酸化的AgNO3,看是否有白色沉淀生成即可;(6)增大铵根的浓度有利于氯化铵析出来,所以选项a正确;通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度,所以选项c正确,选项b错误。 Na2CO3+CO2↑+H2O,故X为CO2;(4)因为氯化钠最后剩余在母液中,所以要提高NaCl的利用率必须将过滤出NaHCO3后的母液循环利用;(5)要检验碳酸钠中是否混有NaCl,只需向溶液中加硝酸酸化的AgNO3,看是否有白色沉淀生成即可;(6)增大铵根的浓度有利于氯化铵析出来,所以选项a正确;通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度,所以选项c正确,选项b错误。 |
相似问题
等量的钠分别完全溶于过量的重水(21H2O)与过量的纯水(11H2O)中。下列有关的叙述中 错误的是
等量的钠分别完全溶于过量的重水(21H2O)与过量的纯水(11H2O)中。下列有关的叙述中,错误的是[ ]A.反应后放出的气体的质量相等B.反应后放出的气体
下列关于100mL 0.1mol/L Na2CO3溶液叙述中不正确的是A.100mL 0.1mol/
下列关于100mL 0 1mol L Na2CO3溶液叙述中不正确的是A.100mL 0 1mol L Na2CO3溶液中含有CO32-的数目小于0 01NAB.热的碳酸钠溶液比冷的碳酸钠溶液洗
我国化工专家侯德榜 改进氨碱法设计了“联合制碱法” 为世界制碱工业作出了突出贡献。生产流程如下:(1
我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。生产流程如下:(1)完成有关反应的化学方程式①沉淀池: NH3+CO
将15.6gNa2O2和5.4gAl同时放入一定量的水中 充分反应后得到200mL澄清溶液 再向该溶
将15 6gNa2O2和5 4gAl同时放入一定量的水中,充分反应后得到200mL澄清溶液,再向该溶液中缓慢通入标准状况下的HCl气体6 72L,若反应过程中溶液的体积保持
下列有关化学实验叙述正确的是( )A.少量金属钠保存在四氯化碳中B.存放浓硝酸时 使用带橡胶塞的棕
下列有关化学实验叙述正确的是()A.少量金属钠保存在四氯化碳中B.存放浓硝酸时,使用带橡胶塞的棕色试剂瓶C.将金属钠投入到足量CuSO4溶液中,静置后












