(5分)某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100g稀硫酸与不同质量的锌粒(
| (5分) 某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
(1)第 次实验,锌粒与稀硫酸恰好完全反应。 (2)计算稀硫酸的质量分数(写出计算过程) |
参考解答
(1)2 (2)9.8% |
| (5分)解:(1)2 ……………………………………………………(1分) (2)用恰好完全反应的第2次实验数据进行计算。 8克锌粒完全反应生成氢气的质量是100g+8g-107.8g =' 0.2g' ……(1分) 设生成0.2g氢气需H2SO4的质量为x Zn + H2SO4 =' ZnSO4' + H2↑ …………………………………………(1分) 98 2 x 0.2g 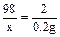 x =' 9.8g ' ………………………………(1分) x =' 9.8g ' ………………………………(1分)该稀硫酸的质量分数为 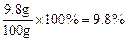 …………………………(1分) …………………………(1分)答:略 |
相似问题
今有H2和O2混合气体100mL 通过电火花使之爆炸 当恢复到原来温度时 水变为液体 气体体积减少至
今有H2和O2混合气体100mL,通过电火花使之爆炸,当恢复到原来温度时,水变为液体,气体体积减少至7mL,则混合气体中H2的体积可能是( )mL:A.69B.67C.33D.62
把26g含有SiO2杂质的碳酸钙在高温下加热到质量不变 冷却后为17.2g 原物质中含碳酸钙____
把26g含有SiO2杂质的碳酸钙在高温下加热到质量不变,冷却后为17 2g,原物质中含碳酸钙______%,最后所得固体由______组成.
欲测定某一部分变质为碳酸钠的氢氧化钠固体中氢氧化钠的含量 小明同学取该样品5.06g放于烧杯中 向其
欲测定某一部分变质为碳酸钠的氢氧化钠固体中氢氧化钠的含量,小明同学取该样品5 06g放于烧杯中,向其中滴加10%的稀盐酸,所加稀盐酸和产生的气体的质量
A和B可发生如下反应:3A+2B====A3B2 某学生做了3次该实验(每次均充分反应) 反应前A和
A和B可发生如下反应:3A+2B====A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量和都是l0克.有关实验数据见右表,X:Y的比值可能为A 1:l
某纯碱产品中含少量的氯化钠 某兴趣小组取12g纯碱样品放入烧杯中 逐滴加入稀盐酸至不再产生气泡为止
某纯碱产品中含少量的氯化钠,某兴趣小组取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸92 4g,烧杯中无残留不溶物,反应后












