A和B可发生如下反应:3A+2B====A3B2 某学生做了3次该实验(每次均充分反应) 反应前A和
| A和B可发生如下反应:3A+2B====A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量和都是l0克.有关实验数据见右表,X:Y的比值可能为 A 1:l B 2:1 C 1: 4 D 3: 2 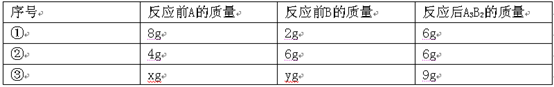 |
参考解答
| D |
| 分析:根据第①次反应和第②次反应进行比较,发现生成物质量相同,每一次反应时有一种物质过量,分析出真正参加反应的A与B的质量比,再根据反应前A和B的质量和都是l0g,分析x:y的值; 解:由题意和图示数据可知,①同学所用药品充分反应时,生成物质量为6.0g故A不可能完全反应,那么B完全反应,A有剩余,故参与反应的A的质量为:6g-2g=4.0g;参与反应的A的质量:B的质量:A3B2量=4:2:6;所以乙同学所用药品充分反应时,A完全反应,B有剩余; A的质量:B的质量:A3B2量=4:2:6,所以③学生如果B充分反应,则B的质量为: yg:9g=2:6 解之得:y=3g, 则反应的x的质量是=10g-3g=7g 则x:y=7:3 如果A完全反应,则A的质量为: xg:9g=4:6 解之得:x=6g, 则反应的y的质量是:y=10g-6g=4g,则x:y=6:4=3:2; 故答案选D |
相似问题
某纯碱产品中含少量的氯化钠 某兴趣小组取12g纯碱样品放入烧杯中 逐滴加入稀盐酸至不再产生气泡为止
某纯碱产品中含少量的氯化钠,某兴趣小组取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡为止,共消耗稀盐酸92 4g,烧杯中无残留不溶物,反应后
现有一块质量为20克的铜锌合金 与足量的稀硫酸完全反应 共生成0.4g氢气 求该铜锌合金中含铜的质量
现有一块质量为20克的铜锌合金,与足量的稀硫酸完全反应,共生成0 4g氢气,求该铜锌合金中含铜的质量分数是多少?
(5004?重庆模拟)将碳酸钠和氯化钠的固化混合物08.9g 完全溶于000g水z 向其z加入000
(5004?重庆模拟)将碳酸钠和氯化钠的固化混合物08 9g,完全溶于000g水z,向其z加入000 8g氯化钡溶液恰好完全反应,过滤,得沉淀的质量为09 7g.求:(0
(10无锡25)一定条件下 在一个密闭容器中发生某反应.测得反应过程中各物质的质量如下表所示物 质X
(10无锡25)一定条件下,在一个密闭容器中发生某反应.测得反应过程中各物质的质量如下表所示物质XYZQ第一次测得的质量/g68164 43 6第二次测得的质量/
电解水时加少量稀H2SO4 可增强水的导电性 但H2SO4 并未反应 现有25克质量分数为8%的稀H
电解水时加少量稀H2SO4,可增强水的导电性,但H2SO4,并未反应,现有25克质量分数为8%的稀H2SO4,通直流电一段时间后,收集到氧气的质量为4 44克,则此时












