某中学课外活动小组在实验室模拟我国化工专家侯德榜先生发明的“联合制碱法”(即“侯氏制碱法”) 其原理
| 某中学课外活动小组在实验室模拟我国化工专家侯德榜先生发明的“联合制碱法”(即“侯氏制碱法”),其原理是向氨化的饱和氯化钠溶液通入足量的二氧化碳,使溶解度较小的碳酸氢钠从溶液中析出,其反应的化学方程式为:NaCl+CO2+NH3+H2O==NH4Cl+NaHCO3。该方法不但可以制得纯碱(将NaHCO3进一步处理即可得到纯碱),还得到优质氮肥氯化氨。 试通过计算回答下列问题: ⑴氯化氨中氮元素的质量分数为_______。(计算结果保留0.1%) ⑵实验中得到碳酸氢钠8.4g,求参加反应的氨气质量为多少? ⑶课外活动小组为了这次模拟实验,准备了8.8g二氧化碳,制取这些二氧化碳需要消耗质量分数为10%的稀盐酸的质量为多少? |
参考解答
| (1)26.2% (2)设参加反应氨气的质量为x。 NaCl+CO2+H2O+NH3==NaHCO3↓+NH4Cl 17 84 x 8.4g 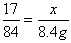 ;x=1.7g ;x=1.7g(3)设消耗质量分数为10%的稀盐酸的质量为y。 CaCO3+2HCl==CaCl2+H2O+CO2↑ 73 44 10%y 8.8g y=146g |
相似问题
同学们从山上采集到一种石灰石 他们取80克该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化) 测得
同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
某校化学兴趣小组同学发现 长期使用的热水壶底部有一层水垢 水垢的主要成分是碳酸钙和氢氧化镁。他们为了
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量质量分数为10
向50.0g8.0%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应。(1)求反应前氢氧化钠溶液中溶质
向50 0g8 0%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应。(1)求反应前氢氧化钠溶液中溶质的质量。(2)求反应后生成硫酸钠的质量。
Fe Mg Al三种金属分别跟稀盐酸充分反应 得到相同质量的氢气 其原因是[ ]A.Fe M
Fe、Mg、Al三种金属分别跟稀盐酸充分反应,得到相同质量的氢气,其原因是[ ]A Fe、Mg、Al的质量相等,盐酸足量 B Fe、Mg、Al的质量比是28∶12∶9,盐酸
高铁酸钠是一种新型净水剂 它的化学式为Na2FeO4 高铁酸钠主要通过如下反应制取:2Fe(OH)3
高铁酸钠是一种新型净水剂,它的化学式为Na2FeO4,高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH==2Na2FeO4+3X+5H2O(1)物质X的化学式为_________












