(6分)一种离子晶体的晶胞如右图其中阳离子A以表示 阴离子B以表示。(1)每个晶胞中含A离子的数目为
(6分)一种离子晶体的晶胞如右图其中阳离子A以 表示,阴离子B以 表示,阴离子B以 表示。 表示。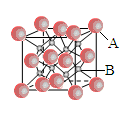 (1)每个晶胞中含A离子的数目为________,含B离子数目为________。 (2)若A的核外电子排布与Ar相同,B的电子排布与Ne相同,则该离子化合物的化学式是___________________; (3)阳离子周围距离最近的阴离子数为_____,阴离子周围距离最近的阳离子数_____。 (4)已知A的离子半径为r m,则该晶胞的体积是 ___________m3。 |
参考解答
| (6分,每空1分)(1)4、8 (2)CaF2 (3)8、4 (4)16r3 |
试题分析:(1)根据晶胞结构可知,B请别再晶胞内,共计是8个。而A离子的个数 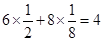 个。 个。(2)根据(1)可知,该离子化合物的化学式是AB2。又因为A的核外电子排布与Ar相同,B的电子排布与Ne相同,则A是Ca,B是F,所以化学式是CaF2。 (3)根据晶胞结构可知,钙离子周围距离最近的阴离子F-数为8个,而阴离子周围距离最近的阳离子数4个。 (4)已知A的离子半径为r m,则该晶胞的面半径是4rm,所以晶胞的边长是 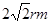 ,因此晶胞的体积是16r3。 ,因此晶胞的体积是16r3。点评:该题是中等难度的试题,也是高考中的重要考点和题型,试题综合性强,注重基础知识的巩固,侧重能力的培养和解题方法的指导与训练。有利于培养学生的逻辑推理能力和抽象思维能力。该题的关键是明确晶胞中离子个数的计算原则和依据,有利于提高学生分析问题、解决问题的能力。 |
相似问题
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物 经过一系列反应可以得到BF3和BN 如下
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:请回答下列问题:(1)由B2O3制备BF3、BN的化学方
有关晶体的下列说法中不正确的是( )A.在NaCl晶体中 距Na+最近的Cl-形成正八面体B.在N
有关晶体的下列说法中不正确的是( )A.在NaCl晶体中,距Na+最近的Cl-形成正八面体B.在NaCl晶体中,每个晶胞平均占有4个Na+C.在CsCl晶体中,每个
下列对各组物质性质的比较中 正确的是A.第一电离能:Na<Mg<AlB.熔点:金刚石>晶体硅>碳化硅
下列对各组物质性质的比较中,正确的是A.第一电离能:Na<Mg<AlB.熔点:金刚石>晶体硅>碳化硅C.硬度:Li>Na>KD.空间利用率:六方密堆<面心立方<
根据表中给出的几种物质的熔 沸点数据 判断下列有关说法中错误的是( ) NaClMgCl2AlC
根据表中给出的几种物质的熔、沸点数据,判断下列有关说法中错误的是()NaClMgCl2AlCl3SiCl4单质B熔点810 ℃710℃190℃—68℃2 300℃沸点1465℃1 418
下列有关晶体的叙述中 错误的是( )A.在SiO2晶体中 每个Si原子与4个O原子形成共价键B
下列有关晶体的叙述中,错误的是()A.在SiO2晶体中,每个Si原子与4个O原子形成共价键B.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金












