(9分)某校一化学实验小组通过实验分析 确定一红色粉末为Fe2O3和Cu2O的混合物。己知:①Cu2
| (9分)某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物。 己知:①Cu2O溶于稀硫酸生成Cu和CuSO4,②Cu2O在空气中加热生成CuO。 (1)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为__________。 (2)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
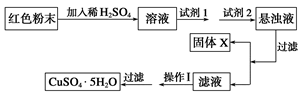 试回答: ①试剂1可以为________________,试剂2可以为________________。 ②固体X的化学式为____________。 ③操作Ⅰ为____________________。 |
参考解答
| (1)×100%(3分) (2)①B;(1分) EF (2分) ②Fe(OH)3(1分) ③蒸发浓缩、冷却结晶(2分) |
(1)氧化亚铜生成氧化铜的方程式为2Cu2O+O2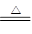 4CuO,所以根据差量法可知,氧化亚铜的质量是 4CuO,所以根据差量法可知,氧化亚铜的质量是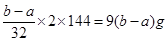 ,所以混合物中Cu2O的质量分数为×100%。 ,所以混合物中Cu2O的质量分数为×100%。(2)①混合物溶液稀硫酸中,生成硫酸铜、铜和硫酸铁,所以应该加入双氧水氧化单质铜,即试剂1是B;试剂2是原来调节溶液pH值的,由于不能引入杂质,所以反应是EF。 ②通过调节pH可以生成氢氧化铁沉淀,则X是Fe(OH)3。 ③要得到硫酸铜晶体,应该通过蒸发浓缩、冷却结晶,最后过滤得到。 |
相似问题
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银 制作美丽的银饰。他们对蚀刻银的
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:[实验]制备银镜,并与Fe(NO3)3溶
(Ⅰ)(8分)某无色溶液中可能含有Na+ SO42— MnO4— Cl— Br— 中的若干种
(Ⅰ)(8分)某无色溶液中可能含有Na+、SO42— 、MnO4—、、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:①用pH试纸检验,溶液pH>
浓H2SO4和木炭在加热时发生反应的化学方程式是请从下图中选用所需的仪器(可重复选用)组成一套进行该
浓H2SO4和木炭在加热时发生反应的化学方程式是请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置。现提供浓H2SO4、木炭和
已知氨可以与灼热的氧化铜反应得到氮气和金属铜 用示意图中的装置可以实现该反应。 回答下列问题:(1)
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。 回答下列问题:(1)A中加入的物质是___________________, 发生反
下图是某化学兴趣小组同学设计的研究铜和稀硝酸反应速率[υ(NO)]的实验装置图。试回答下列问题(1)
下图是某化学兴趣小组同学设计的研究铜和稀硝酸反应速率[υ(NO)]的实验装置图。试回答下列问题(1)写出铜和稀硝酸反应的离子方程式____________________












