烧杯中盛有100 mL 1 mol/L的NaHSO4溶液 向其中逐滴滴加1 mol/L的Ba(OH)
烧杯中盛有100 mL 1 mol/L的NaHSO4溶液,向其中逐滴滴加1 mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图。下列说法中正确的是( )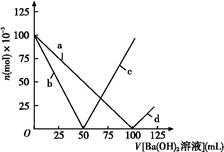
|
参考解答
| B |
起始n(NaHSO4)='0.1' mol,即n(Na+)='0.1' mol[反应前后n(Na+)不变,所以曲线不对应Na+,n(H+)='0.1' mol,n(SO42—)='0.1' mol,加入Ba(OH)2溶液后,SO42—、H+要减少,加入Ba(OH)2溶液50 mL时,即n[Ba(OH)2='0.05' mol,此时H+中和完,所以曲线b表示H+的变化,SO42—反应一半,当加入Ba(OH)2溶液大于50 mL时,OH-开始增多,所以曲线c表示OH-的变化,当加入Ba(OH)2溶液100 mL时,SO42—沉淀完,所以曲线a表示SO42—的变化,加入Ba(OH)2溶液大于100 mL时,Ba2+开始增多,所以曲线d表示Ba2+的变化,加入Ba(OH)2溶液50 mL 时,反应的H+与SO42—的物质的量之比为2∶1,所以离子方程式为:Ba2++2OH-+2H++SO42— 2H2O+BaSO4↓,大于50 mL 时,H+已反应完,反应为Ba2++SO42— 2H2O+BaSO4↓,大于50 mL 时,H+已反应完,反应为Ba2++SO42— BaSO4↓。 BaSO4↓。 |
相似问题
下列化学方程式及离子方程式中 正确的是( )A.钠与CuSO4溶液反应:2Na+Cu2+=Cu+
下列化学方程式及离子方程式中,正确的是()A.钠与CuSO4溶液反应:2Na+Cu2+=Cu+2Na+B.等物质的量的NaHCO3溶液和Ba(OH)2溶液混合:HCO3-+Ba2++OH-=
下列方程式中正确的是A.FeCl2溶液滴加碘水:2Fe2++I2=2Fe3++2I—B.双氧水中滴加
下列方程式中正确的是A.FeCl2溶液滴加碘水:2Fe2++I2=2Fe3++2I—B.双氧水中滴加2滴FeCl3溶液:2Fe3++H2O2=2Fe2++O2↑+2H+C.双氧水加入稀硫酸和KI溶液:
下列反应属于氧化还原反应的是[ ]A. CaCO3+2HCl=CaCl2+H2O+CO2↑B
下列反应属于氧化还原反应的是[ ]A CaCO3+2HCl=CaCl2+H2O+CO2↑B 2NaHCO3Na2CO3+H2O+CO2↑C Cl2+2NaOH=NaCl+NaClO+H2O D NaBr+AgNO3=AgBr↓+NaNO3
下列离子方程式正确的是A.钠与水反应:Na + 2H2O = Na+ + 2OH- + H
下列离子方程式正确的是A.钠与水反应:Na + 2H­2O = Na+ + 2OH- + H2↑B.硅酸钠溶液与醋酸溶液混合:SiO32- + 2H+ = H2SiO3↓C.0 0
向Ba(OH)2溶液中逐滴加入稀硫酸 请完成下列问题:(1)写出反应的离子方程式:
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:(1)写出反应的离子方程式:。(2)下列三种情况下,离子方程式与 (1)相同的是(填序号)。A.向NaHSO4溶液












