向Ba(OH)2溶液中逐滴加入稀硫酸 请完成下列问题:(1)写出反应的离子方程式:
| 向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题: (1)写出反应的离子方程式: 。 (2)下列三种情况下,离子方程式与 (1)相同的是 (填序号)。 A.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性 B.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀 C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 (3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用如图中的 (填序号)曲线表示。 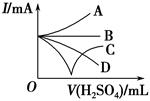 (4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示。向该烧杯中缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将 。 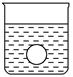 |
参考解答
| (1)Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O (2)A (3)C (4)下沉 |
| (1)向Ba(OH)2溶液中逐滴加入稀硫酸,反应的离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O。(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液显中性,反应的离子方程式为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,离子方程式为:Ba2++OH-+SO42-+H+=BaSO4↓+H2O;向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量,反应的离子方程式为:H++SO42-+Ba2++OH-=BaSO4↓+H2O。(3)向Ba(OH)2溶液中缓缓加入稀硫酸,当Ba(OH)2与H2SO4恰好完全反应时,溶液导电能力接近为零,再加过量稀硫酸,溶液导电能力又增强,故曲线C正确。(4)Ba(OH)2与H2SO4反应过程中,随反应的进行,溶液密度变小,塑料小球下沉。 |
相似问题
以冶铝的废弃物铝灰为原料制取超细α-氧化铝 既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分
以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制
解释下列事实的方程式不正确的是A.次氯酸钙溶液中通入过量二氧化硫:Ca2+ + 2ClO-+ H2O
解释下列事实的方程式不正确的是A.次氯酸钙溶液中通入过量二氧化硫:Ca2+ + 2ClO-+ H2O + SO2=CaSO3↓+ 2HClOB.硫酸型酸雨放置一段时间溶液的p
从海水中提取溴的反应原理是5NaBr + NaBrO3 + 3H2SO4 == 3Br2 + 3Na
从海水中提取溴的反应原理是5NaBr + NaBrO3 + 3H2SO4 == 3Br2 + 3Na2SO4 + 3H2O,下列反应的原理与上述反应最相似的是 [ ]A.2NaBr + Cl2
下列关于氧化还原反应应用的说法不正确的是[ ]A.在农业生产中 植物的光合作用 呼吸作用是复
下列关于氧化还原反应应用的说法不正确的是[ ]A.在农业生产中,植物的光合作用、呼吸作用是复杂的氧化还原反应 B.我们通常使用的干电池、蓄电池以及
下列离子方程式正确的是( )A.过氧化钠和水反应:2Na2O2+2H2O=4Na++4 O
下列离子方程式正确的是( )A.过氧化钠和水反应:2Na2O2+2H2O=4Na++4 OH—+O2↑B.用铜为电极电解饱和食盐水:2Cl—+2H2O通电Cl2↑+H2↑+2OH—C.在明












