(15分)亚硝酸钠(NaNO2)易溶于水 微溶于乙醚 是常用的食品发色剂(1)第一电离能:N ___
| (15分) 亚硝酸钠(NaNO2)易溶于水,微溶于乙醚,是常用的食品发色剂 (1)第一电离能:N ___O(填“<”、“>”或“=”);NO2-的空间构型为____ (2)亚硝酸钠在3200C会分解生成氧化钠、一氧化二氮等物质,该反应的化学方程式为____ (3)亚硝酸钠是亚硝酸的钠盐。HNO2的结构如图所示,则HNO2分子中有___个 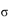 键: 键:HNO2的酸性比HN03弱是因为_____ 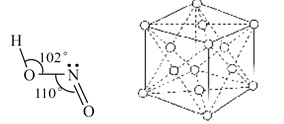 (4)亚硝基钻钠 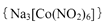 是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的 是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的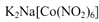 沉淀,可用于检验K+的存在。 沉淀,可用于检验K+的存在。①基态 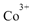 的价层电子排布图为_____ 的价层电子排布图为_____②用亚硝酸钻钠检验K+的离子方程式是 ③金属钴的堆积方式如图所示,若一个钴原子的半径为r,,则晶胞的体积V(晶胞)=__ |
参考解答
| (15分) (1) > (1分) V型或角型(1分) (2)2NaNO2  Na2O+N2O↑+O2↑(2分) Na2O+N2O↑+O2↑(2分)(3)3(2分) HNO3中的N的正电性高,导致N—O—H中O的电子向N偏移程度大于HNO3,更容易电离出H+,酸性更强(3分) 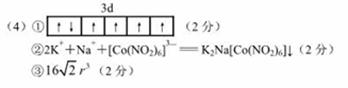 |
试题分析:(1)因为N元素为VA族元素,N原子2p轨道排布3个电子,为半充满状态,为较稳定状态,失去电子较难,所以第一电离能:N > O;NO2-中N价电子为5,所以杂化轨道数=(5+1)÷2=3,所以N原子杂化方式为sp2,所以NO2-的空间构型为V型或角型。 (2)亚硝酸钠在3200C会分解生成氧化钠、一氧化二氮等物质,配平可得化学方程式:2NaNO2  Na2O +N2O↑+O2↑ Na2O +N2O↑+O2↑(3)单键为 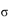 键,双键中的一个键为 键,双键中的一个键为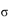 键,根据HNO2的结构简式可知HNO2分子中有3个 键,根据HNO2的结构简式可知HNO2分子中有3个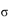 键;HNO3中的N的正电性高,导致N—O—H中O的电子向N偏移程度大于HNO3,更容易电离出H+,酸性更强。 键;HNO3中的N的正电性高,导致N—O—H中O的电子向N偏移程度大于HNO3,更容易电离出H+,酸性更强。(4)①Co为27号元素,Co3+的价层电子为3d6,所以基态Co3+的3d轨道有1个排布2个电子,其它4个轨道排布1个电子。 ②根据亚硝基钻钠{Na3[Co(NO2)6与钾离子反应生成淡黄色的K2Na[Co(NO2)6沉淀,可得离子方程式为:2K++Na++[Co(NO2)63- = K2Na[Co(NO2)6↓ ③根据钴晶体堆积方式可知,其晶胞为面向立方,面对角线等于4r,设晶胞的边长为a,则4r= 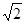 a,可得a=2 a,可得a=2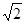 r,则晶胞的体积V(晶胞)=a3=(2 r,则晶胞的体积V(晶胞)=a3=(2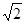 r)3=16 r)3=16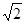 r3。 r3。 |
相似问题
美国科学家将两种元素铅和氪的原子核对撞 获得了一种质子数118 中子数为175的超重 元素 该元素
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重元素,该元素原子核内中子数与核外电子数之差是() A.57B.47C.61D.293
从宏观方面看物质是由元素组成的 从微观方面看物质是由粒子构成的 下列有关说法不正确的是( )A.元
从宏观方面看物质是由元素组成的,从微观方面看物质是由粒子构成的,下列有关说法不正确的是()A.元素原子的多样性是由构成原子的质子和中子数目引起的
(12分)【化学-物质结构与性质】原子序数依次增大的A B C D E F六种元素。其中A的基态原子
(12分)【化学-物质结构与性质】原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p
下列说法正确的是A.中国是目前全球最大的稀土提炼和加工国 对稀土元素及其化合物的研究是获得优良催化剂
下列说法正确的是A.中国是目前全球最大的稀土提炼和加工国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径B.气化、液化和干馏是煤综合利
下列事实中 能说明氯的非金属性比硫强的是 A.高氯酸的酸性比亚硫酸强B.次氯酸的氧化性比稀硫酸强C.
下列事实中,能说明氯的非金属性比硫强的是 A.高氯酸的酸性比亚硫酸强B.次氯酸的氧化性比稀硫酸强C.氯化氢比硫化氢的热稳定性好D.氯原子最外层电子












