将下列物质按照要求由高到低的顺序排列(1)NaF NaCl 冰醋酸 SiC四种物质的熔沸点顺序:
| 将下列物质按照要求由高到低的顺序排列 (1)NaF、NaCl、冰醋酸、SiC四种物质的熔沸点顺序: 。 (2)C、N、O三种元素的第一电离能: 。 (3)H2O的相对分子质量比H2S小,但沸点却高的原因 。 (4)某气态团簇分子的分子结构如图所示,其晶体的晶胞与CO2晶体的晶胞类型相同,则该团簇分子的分子式为 。 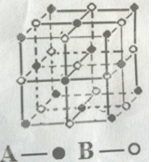 |
参考解答
| (1)SiC> NaF> NaCl>冰醋酸; (2)N>O>C; (3)水分子间存在氢键使分子间作用力增大,沸点升高; (4)AB或BA。 |
试题分析:(1)根据晶体类型的熔沸点的高低顺序,原子晶体>离子晶体>分子晶体,离子晶体中,离子半径越小,熔沸点越高。所以四种物质熔沸点由高到低的顺序SiC> NaF> NaCl>冰醋酸; (2)同周期元素的第一电离能随核电荷数增加而增大,但是氮原子的最外层电子为半充满状态,比较稳定,所以第一电离能最大,因此C、N、O三种元素的第一电离能N>O>C; (3)水分子间存在氢键使分子间作用力增大,沸点升高; (4)由晶胞中原子个数的计算方法得该晶胞中有8×1/8+6×1/2=4个A,有12×1/4+1=4个B,所以AB的原子个数比为1:1,分子式为AB或BA。 |
相似问题
元素R X T Z Q在元素周期表中的相对位置如下表所示 其中R单质在暗处与H2剧烈化合并发生爆炸
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是A.非金属性:Z<T<XB.R与Q的电
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象.试判断下列哪组原子均可产
如图为元素周期表中短周期的一部分 四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( ) A.原子半径:W>Z>Y>XB.气态氢化
元素的种类和原子的种类( )。A.前者多B.后者多C.相同D.无法确定
元素的种类和原子的种类( )。A.前者多B.后者多C.相同D.无法确定
在通常条件下 下列各组物质的性质排列不正确的是( )A.熔点:CO2
在通常条件下,下列各组物质的性质排列不正确的是( )A.熔点:CO2<KCl<SiO2B.沸点:乙烷>戊烷>2­甲基丁烷C.密度:苯<水<1,1,2,2­四溴乙烷D












