【物质结构与性质】碳 氮 氧是构成生命物质的三种主要元素。(1)碳 氮 中 原子核外电子未成对电子数
| 【物质结构与性质】 碳、氮、氧是构成生命物质的三种主要元素。 (1)碳、氮、中,原子核外电子未成对电子数最多的是 (用元素符号表示)。 (2)已知CN-与N2结构相似,则HCN分子中σ键与π键数目之比为 。 (3)H2O2分子中氧原子的杂化方式为 。 (4)与NO2+互为等电子体的微粒有 、 (举2例),NO3-的空间构型是 。 (5)已知元素A的氧化物的晶胞结构如图所示,则该氧化物的化学式为 。 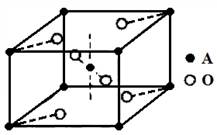 |
参考解答
| (1)N (2)1:1 (3)sp3 (4)CO2、N2O、CNO-、SCN-等;平面三角形 (5)AO2 |
| (1)根据核外电子排布规律可知,碳、氮、氧三种元素的核外电子排布分别为1s22s22p2、1s22s22p3、1s22s22p4,因此原子核外电子未成对电子数最多的是N元素。 (2)已知CN-与N2结构相似,因些HCN分子结构式为H-C≡N,σ键与π键之比是1:1。 (3)H2O2分子中氧原子分别形成2个单键,另外还原2对孤对电子,所以氧原子的价层电子对数是4,因此氧原子的杂化类型是sp3。 (4)原子数和价电子数分别都相等的互为等电子体,则与NO2-互为等电子的微粒有CO2、N2O、CNO-、SCN-等;NO3-含有的孤电子对数是(5+1-3×2)=0,所以它的空间构型是平面三角形。 (5)根据晶胞结构知,A原子数是=1+8×1/8=2,O原子数=2+4×1/2=4,则该氧化物的化学式为AO2。 |
相似问题
已知X+ Y2+ Z- W2-四种离子均具有相同的电子层结构。下列关于X Y Z W四种元素的描述
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,不正确的是()A.原子序数:Y>X>Z>WB.离子半径: X+>Y2+>Z-
铊是超导材料的组成元素之一 铊在周期表中位于第六周期 与铝是同族元素 元素符号是Tl 以下对铊的性质
铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是A.铊是易导电的银白色金属B.
短周期元素A B C D的原子序数依次增大 A的原子半径在所有原子中最小 B位于第VA族 A和C同主
短周期元素A、B、C、D的原子序数依次增大,A的原子半径在所有原子中最小,B位于第VA族,A和C同主族,D原子最外层电子数与电子层数相等。下列叙述正确的是
已知X为第三周期元素的原子 该原子要达到8电子稳定结构 则需要的电子数小于其次外层和最内层的电子数之
已知X为第三周期元素的原子,该原子要达到8电子稳定结构,则需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确
甲 乙两种非金属性质比较:①甲的单质熔 沸点比乙的低;②甲单质能氧化乙原子的阴离子;③最高价氧化物对
甲、乙两种非金属性质比较:①甲的单质熔、沸点比乙的低;②甲单质能氧化乙原子的阴离子;③最高价氧化物对应的水化物酸性比较,甲比乙的强;④与金属反












