R2O8n-离子在一定条件下可把Mn2+氧化成 若反应后变成 且反应中氧化剂与还原剂的离子个数比为5
R2O8n-离子在一定条件下可把Mn2+氧化成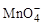 ,若反应后 ,若反应后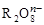 变成 变成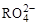 ,且反应中氧化剂与还原剂的离子个数比为5:2,则R2O8n-中R元素的化合价以及n分别为 ,且反应中氧化剂与还原剂的离子个数比为5:2,则R2O8n-中R元素的化合价以及n分别为
|
参考解答
| A |
| : 试题分析:R2O8n-中R化合价为+(8- 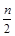 ),Mn2+是还原剂,R2O8n-是氧化剂,根据得失电子相等得:5×2×(8- ),Mn2+是还原剂,R2O8n-是氧化剂,根据得失电子相等得:5×2×(8-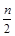 -6)=2×(7-2) -6)=2×(7-2)解得:n=2。R2O82-中R化合价为+7。 点评:氧化还原反应计算关键是得失电子相等。 |
相似问题
将a g纯铜片投入足量的一定浓度的硝酸溶液中 反应中消耗的HNO3为b g.若a∶b=8∶21 则反
将a g纯铜片投入足量的一定浓度的硝酸溶液中,反应中消耗的HNO3为b g.若a∶b=8∶21,则反应中起酸性作用的硝酸的质量为( )。
氯气用途广泛 可用于生产半导体硅 生产的流程如下 下列说法不正确的是A.①③是置换反应 ②是化合反应
氯气用途广泛,可用于生产半导体硅,生产的流程如下,下列说法不正确的是A.①③是置换反应,②是化合反应B.高温下,焦炭与氢气的还原性均强于硅C.任一
在一定条件下 RO3n-和I-可发生如下反应:RO3n- +6I-+6H+ = R-+ 3I2 +3
在一定条件下,RO3n-和I-可发生如下反应:RO3n- +6I-+6H+ = R-+ 3I2 +3H2O,则RO3n-中R元素的化合价为:()A.+1B.+3C.+5D.+7
实验室用MnO2和浓HCl加热制取Cl2时 有14.6gHCl被氧化 将所得气体全部用石灰水吸收 可
实验室用MnO2和浓HCl加热制取Cl2时,有14.6gHCl被氧化,将所得气体全部用石灰水吸收,可得漂白粉质量是A.14.3gB.25.4gC.28.6gD.50.6g
请将5种物质:N2O FeCl2 Fe (NO3)3 HNO3和FeCl3分别填入下面对应的横线上
请将5种物质:N2O、FeCl2、Fe (NO3)3、HNO3和FeCl3分别填入下面对应的横线上,组成一个未配平的化学方程式。(1)_________+__________→__________+___












