(11分)回答下列问题(1)在2FeBr2+3Cl2=2FeCl3+2Br2的反应中 被氧化的元素是
| (11分)回答下列问题 (1)在2FeBr2+3Cl2=2FeCl3+2Br2的反应中,被氧化的元素是_____________ (2)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液(FeCl2);浓盐酸中滴加KMnO4溶液产生黄绿色气体(Cl2)。则Cl2、Fe3+、MnO4-氧化性由强到弱的顺序是____________________。 (3)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式____________________________________________。 (4)在一定条件下,RO3n-和Cl2可发生如下反应:RO3n-+Cl2+2OH-=RO42-+2Cl-+H2O 由以上反应可知在上述过程中RO3n-被________________(填“氧化”或“还原”),RO3n-中元素R的化合价是______________。 |
参考解答
| (11分)(1)Fe(2分)和Br(2分) (2)MnO4->Cl2>Fe3+ (2分) (3)3CuO+2NH3 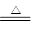 3Cu+N2+3H2O(2分)(4)氧化(1分) +4(2分) 3Cu+N2+3H2O(2分)(4)氧化(1分) +4(2分) |
试题分析:(1)根据反应的方程式可知,溴化铁中铁元素的化合价从+2价升高到+3价,被氧化。而溴元素的化合价溴-1价升高到0价,被氧化。 (2)在氧化还原反应中氧化剂的氧化性强于氧化产物的,所以反应中的实验现象可判断,Cl2、Fe3+、MnO4-氧化性由强到弱的顺序是MnO4->Cl2>Fe3+。 (3)因为氧化铜具有氧化性,所以根据原子守恒可知,两种单质应该是氮气和铜,则反应的化学方程式是3CuO+2NH3 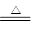 3Cu+N2+3H2O。 3Cu+N2+3H2O。(4)氯元素的化合价降低,所以氯气是氧化剂,则RO3n-被氧化,作还原剂。RO42-中R元素的化合价是+6价,所以根据电子的得失守恒可知,RO3n-中元素R的化合价是+(6-2)=+4价。 点评:该题是中等难度的试题,试题基础性强,侧重能力的培养。该题的关键是准确标出有关元素的化合价变化情况,然后根据氧化还原反应的有关概念灵活运用、计算判断即可。 |
相似问题
已知离子方程式:As2S3+H2O+NO3—―→AsO43—+SO42—+NO↑+______K(未
已知离子方程式:As2S3+H2O+NO3—―→AsO43—+SO42—+NO↑+______K(未配平),下列说法错误的是( )。A.配平后水的化学计量数为4B.反应后溶液呈
已知:还原性HSO3¯>I¯ 氧化性IO3¯> I2。在含3 mol
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所
对剧毒的氰化物可在碱性条件下用如下方法进行处理:2CN- +8OH-+5Cl2= 2CO2 +N2
对剧毒的氰化物可在碱性条件下用如下方法进行处理:2CN- +8OH-+5Cl2= 2CO2 +N2 +10Cl- +4H2O 下列判断正确的是A.当有0 2 mol CO2生成时,溶液中
Na2FeO4是一种高效多功能水处理剂 应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式
Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4 + 6Na2O2 = 2Na2FeO4 + 2Na2O + 2
铜和镁的合金4.6g完全溶于浓硝酸 若反应中硝酸被还原只产生4480mL的NO2气体和336mlN2
铜和镁的合金4 6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mlN2O4(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠












