汽车安全气囊是行车安全的重要保障.当车辆发生碰撞的瞬间 安全装置通电点火使其中的固体粉末分解释放出大
| 汽车安全气囊是行车安全的重要保障.当车辆发生碰撞的瞬间,安全装置通电点火使其中的固体粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客免受伤害.为研究安全气囊工作的化学原理,取安全装置中的固体粉末进行实验.经组成分析,确定该粉末仅含Na、Fe、N、O四种元素.水溶性实验表明,固体粉末部分溶解.经检测,可溶物为化合物甲;不溶物为红棕色固体,可溶于盐酸.取13.0 g化合物甲,加热使其完全分解,生成氮气和单质乙,生成的氮气折合成标准状况下的体积为6.72 L.单质乙在高温隔绝空气的条件下与不溶物红棕色粉末反应生成化合物丙和另一种单质.化合物丙与空气接触可转化为可溶性盐.请回答下列问题: (1)甲的化学式为____________,丙的电子式为____________. (2)若丙在空气中转化为碳酸氢盐,则反应的化学方程式为_____________________. (3)单质乙与红棕色粉末发生反应的化学方程式为___________________________,安全气囊中红棕色粉末的作用是_________________________________. (4)以下物质中,有可能作为安全气囊中红棕色粉末替代品的是________. A.KCl B.KNO3 C.Na2S D.CuO (5)设计一个实验方案,探究化合物丙与空气接触后生成可溶性盐的成分(不考虑结晶水合物)______________________________________________________________________________________________________________________. |
参考解答
(1)NaN3;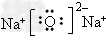 (2)Na2O+2CO2+H2O==2NaHCO3 (3)6Na+Fe2O3  2Fe+3Na2O;避免分解产生的金属钠可能产生的危害 2Fe+3Na2O;避免分解产生的金属钠可能产生的危害(  4)BD 4)BD(5)可溶性盐的成分可能是Na2CO3,或NaHCO3,或Na2CO3与NaHCO3的混合物.准确称取一定量的生成物,加热至恒重后,如试样无失重,则为Na2CO3;如加热后失重,根据失重的量在试样总质量中的比例,即可推断出试样为NaHCO3,或Na2CO3与NaHCO3的混合物. |
相似问题
A B C D E均为可溶于水的固体 组成它们的离子有阳离子Na+ Mg2+ Al3+ Ba2+阴离
A、B、C、D、E均为可溶于水的固体,组成它们的离子有阳离子Na+、Mg2+、Al3+、Ba2+阴离子OH-、Cl-、CO32-、SO42-、HSO4-分别取它们的水溶液进行实验.结果
化学中有许多物质之间的反应符合如图关系图 图中其他产物及反应所需条件均已略去.下列说法正确的是(
化学中有许多物质之间的反应符合如图关系图,图中其他产物及反应所需条件均已略去.下列说法正确的是( )A.若X、Y为Fe,Z是氢氧化钠则D可能为氢氧化
元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化.则X为( )A.当n=1时 X可能是M
元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化.则X为( )A.当n=1时,X可能是MgB.当n=1时,X可能是N2C.当n=2时,X可能是SD.当n=2时,X可能是Fe
能实现下列物质间直接转化的元素是( )单质+O2氧化物+H2O酸或碱+NaOH或HCl盐.A.硅B
能实现下列物质间直接转化的元素是( )单质+O2氧化物+H2O酸或碱+NaOH或HCl盐.A.硅B.氮C.钠D.铁
已知A B为单质 C为化合物。能实现上述转化关系的是①若C溶于水后得到强碱溶液 则A可能是Na ②若
已知A、B为单质,C为化合物。能实现上述转化关系的是①若C溶于水后得到强碱溶液,则A可能是Na ②若C溶液遇Na2CO3,放出CO2气体,则A可能是H2③若C溶液中












