(14分)实验和探究对化学学科的发展起着非常重要的作用(1)写出下列实验过程中所体现的总的离子反应方
| (14分)实验和探究对化学学科的发展起着非常重要的作用 (1)写出下列实验过程中所体现的总的离子反应方程式: ①用PH试纸测得醋酸钠溶液呈碱性:__________ ②用石墨做电极,电解硝酸银溶液后,溶液呈酸性:__________ ③根据浑浊出现的快慢,探究硫代硫酸钠与酸反应速率的影响因素:__________ (2)已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6 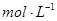 NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为 NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为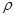 ,则h=__________ ,则h=__________(3)实验室测定绿矾中FeSO4 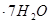 含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有: 含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有: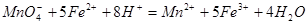 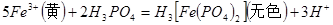 ①绿矾的含量为__________%。 ② 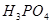 的作用是__________。 的作用是__________。 |
参考解答
(1)①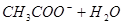  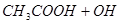 ② 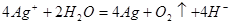 ③ 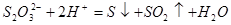 (2)产生氢气速率突然变慢 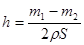 (3)2.78V% 消除 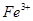 的颜色干扰 的颜色干扰 |
(1)①醋酸钠是强碱弱酸盐,水解显碱性,方程式为CH3COO-+H2O CH3COOH+OH-。 CH3COOH+OH-。②用石墨做电极,电解硝酸银溶液后,阳极OH-放电,生成氧气,从而破坏水的电离平衡,因此溶液中氢离子大于OH-浓度,显酸性,方程式为4Ag++2H2O  4Ag+4H++O2↑。 4Ag+4H++O2↑。③在酸性条件下,硫代硫酸钠发生氧化还原反应生成单质S和SO2,方程式为 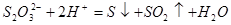 。 。(2)当锌完全被消耗之后,溶液中就不再产生氢气,即产生氢气的速率突然变慢时,就说明反应已知停止。参加反应的锌是m1-m2,所以有2hS=m1-m2,解得h= 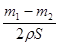 。 。(3)①消耗高锰酸钾是2V×10-5mol,所以绿矾的物质的量是2V×10-5mol×5=V×10-4mol,所以含量是 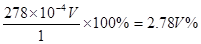 . .②由于铁离子在溶液中显棕黄色,能干扰终点的颜色判断,所以磷酸的作用是消除 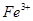 的颜色干扰。 的颜色干扰。 |
相似问题
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究。(1)写出试管B中的实验现象_________
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究。(1)写出试管B中的实验现象______________________。 (2)写出A中反应的化学方程式_________
(12分)某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。(1)提出假设:①该反应的气
(12分)某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。(1)提出假设:①该反应的气体产物是CO2;②该反应的气体产物是CO;③该反应的
科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。 (1)四种制取Cu2O的方法(a)用炭粉在
科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。 (1)四种制取Cu2O的方法(a)用炭粉在高温条件下还原CuO制备Cu2O;(b)用葡萄糖还原新制的Cu(
某研究性学习小组用FeCl3溶液做“腐蚀液” 制作印刷电路板 其反应原理是:2FeCl3+Cu=2F
某研究性学习小组用FeCl3溶液做“腐蚀液”,制作印刷电路板,其反应原理是:2FeCl3+Cu=2FeCl2+CuCl2。【实验探究】(1)通过《化学1》的学习,知道了有离
某化学兴趣小组欲研究一种镁铝合金 以下是部分实验。请完成填空。1 [实验一]从镁铝合金片上剪下一小块
某化学兴趣小组欲研究一种镁铝合金,以下是部分实验。请完成填空。1、[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol·L-1NaOH溶液












