镍(Ni)可形成多种配合物 且各种配合物均有广泛的用途。(1)配合物Ni(CO)4常温下呈液态 易溶
| 镍(Ni)可形成多种配合物,且各种配合物均有广泛的用途。 (1)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于________晶体;写出两种与配体CO互为等电子体的粒子的化学式________、________。 (2)某镍配合物结构如下图所示,分子内含有的作用力有________(填序号)。 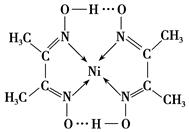
①  ② ② 、③ 、③ 、④ HCHO等,其中碳原子采取sp2杂化的分子有________(填序号);HCHO分子的空间构型为________ 。 、④ HCHO等,其中碳原子采取sp2杂化的分子有________(填序号);HCHO分子的空间构型为________ 。(4)据报道,含有镁、镍和碳三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为________。晶体中每个镁原子周围距离最近的镍原子有________个。 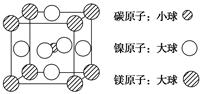 |
参考解答
| (共12分) (1)分子 (1分) N2(1分)CN-(1分) (2)ACE(2分) (3)①③④(2分) 平面三角形(1分) (4)MgNi3C(2分) 12(2分) |
| (1)根据相似相溶原理可知,化合物是非极性分子,所以形成的晶体是分子晶体。电子数和原子数分布都相等的分子是等电子体,所以和CO互为等电子体的是氮气或CN-。 (2)根据配合物结构可判断,分子中不存在离子键和金属键,所以答案选ACE。 (3)①③④都是平面型结构,所以是sp2杂化。乙炔是直线型结构,是sp杂化。HCHO分子中碳原子没有孤对电子,是sp2杂化,所以是平面三角形结构。 (4)根据晶胞的结构可知,碳原子全部在晶胞中,共有1个。镁原子在面心处,共有6×1/2=3个。镍原子在顶点处,共有8×1/8=1个,所以化学式为MgNi3C。晶体中每个镁原子周围距离最近的镍原子位于面心处,所以共有3×8÷2=12个。 |
相似问题
(14分)X Y Z三种元素 原子序数依次减小。X是第四周期主族元素 其部分电离能如图17所示;X
(14分)X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图17所示;X、Y元素具有相同的最高正化合价;Z元素是形成化合物种类最
氮化钠和氢化钠都是离子化合物 与水反应的化学方程式(未配平)如下:Na3N+H2O→NaOH+NH3
氮化钠和氢化钠都是离子化合物,与水反应的化学方程式(未配平)如下:Na3N+H2O→NaOH+NH3 NaH+H2O→NaOH+H2有关它们的叙述正确的是A.离子半径:N3—>
类推的思维方法在化学学习与研究中常会产生错误的结论。因此类推出的结论最终要经过实践的检验才能确定其正
类推的思维方法在化学学习与研究中常会产生错误的结论。因此类推出的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中正确的是()A.从
(5分)现有下列物质 用编号填空回答下列各问题:A.干冰B.金刚石C.氩D.过氧化钠 E.二氧化硅
(5分)现有下列物质, 用编号填空回答下列各问题:A.干冰B.金刚石C.氩D.过氧化钠 E.二氧化硅 F.氯化铵(1)通过非极性键形成的晶体是 。(
下列叙述中的距离属于键长的是( )A.氨分子中两个氢原子间的距离B.氯分子中两个氯原子间的距离
下列叙述中的距离属于键长的是( )A.氨分子中两个氢原子间的距离B.氯分子中两个氯原子间的距离C.金刚石晶体中任意两个相邻的碳原子核间的距离D.氯化












