甲 乙 丙 丁为前三周期元素形成的粒子 它们的电子总数相等。已知甲 乙 丙为双原子分子或负二价双原
| 甲、乙、丙、丁为前三周期元素形成的粒子,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。 (1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是______________________________。 (2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途: ________________________________________。 (3)在一定条件下,甲与O2反应的化学方程式是______________________________。 (4)丁的元素符号是__________,它的原子结构示意图为__________。 (5)丁的氧化物的晶体结构与__________的晶体结构相似。 |
参考解答
| (1)CaC2+2H2O====C2H2↑+Ca(OH)2 (2)答案略。(只要考生的答案符合题意要求,即可给分) (3)N2+O2  2NO 2NO(4)Si 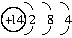 (5)金刚石 |
| 根据题意第(1)问题中的信息可知CaC2与H2O反应,确定丙为C2-2,因此可以确定甲、乙、丙、丁均为14电子粒子,丁为原子,可确定为Si ,乙在高温下为工业上一种重要的还原剂,可确定为CO,甲为N2,SiO2为原子晶体,与金刚石的晶体结构相似。 |
相似问题
下列说法中正确的是( )A.金刚石晶体中的最小碳原子环由6个碳原子构成B.Na2O2晶体中阴离
下列说法中正确的是( )A.金刚石晶体中的最小碳原子环由6个碳原子构成B.Na2O2晶体中阴离子与阳离子数目之比为1∶1C.1 mol SiO2晶体中含2 mol Si—
石墨晶体中不存在的化学作用力是( )A.共价键B.氢键C.金属键D.范德华力
石墨晶体中不存在的化学作用力是( )A.共价键B.氢键C.金属键D.范德华力
金属的下列性质中 不能用电子气理论加以解释的是( )A.易导电B.易导热C.有延展性D.易锈蚀
金属的下列性质中,不能用电子气理论加以解释的是( )A.易导电B.易导热C.有延展性D.易锈蚀
(18分)根据下图回答问题:(1)A图是某离子化合物的晶胞(组成晶体的一个最小重复单位) 阳离子位于
(18分)根据下图回答问题:(1)A图是某离子化合物的晶胞(组成晶体的一个最小重复单位),阳离子位于中间,阴离子位于8个顶点,该化合物中阳、阴离子的个数比
(8分)锡有白锡和灰锡两种单质 常见的白锡银白色有金属光泽 密度7.31g/cm3 软而富有展性 导
(8分)锡有白锡和灰锡两种单质,常见的白锡银白色有金属光泽,密度7 31g cm3,软而富有展性,导电导热能力强,在13 2℃---161℃间稳定。白锡剧冷转变为












